Блокаторы н2 гистаминовых рецепторов
Содержание:
Личный опыт
Вероятно, у каждого врача есть собственный фармакотерапевтический справочник, отражающий его личный клинический опыт применения препаратов, пристрастия и негативное отношение. Успех применения лекарства у одного-трех-десяти первых пациентов обеспечивает пристрастие к нему врача на многие годы, а литературные данные укрепляют мнение о его эффективности. Привожу список некоторых современных бета-блокаторов, на которые у меня есть свой опыт клинического применения.
Пропранолол
Первый из бета-блокаторов, который я стал применять в своей практике. Кажется, в середине 70‑х годов прошлого века пропранолол был чуть ли не единственным бета-блокатором в мире и уж точно — единственным в СССР. Препарат до сих пор относится к наиболее часто назначаемым среди бета-блокаторов, имеет больше показаний к применению по сравнению с другими бета-блокаторами. Однако, применение его в настоящее время я не могу считать оправданным, т. к. другие бета-блокаторы имеют гораздо менее выраженные побочные эффекты.
Пропранолол можно рекомендовать в комплексной терапии ишемической болезни сердца, он также эффективен для снижения артериального давления при гипертонической болезни. При назначении пропранолола существует риск развития ортостатического коллапса
Пропранолол с осторожностью назначают при сердечной недостаточности, при фракции выброса менее 35 % препарат противопоказан.
По моим наблюдениям, пропранолол эффективен при лечении пролапса митрального клапана: дозировки 20–40 мг в сутки достаточно, чтобы пролабирование створок (обычно передней) исчезло или существенно уменьшилось с третьей-четвертой степени до первой или нулевой.
Бисопролол
Кардиопротективный эффект бета-блокаторов достигается при дозировке, которая обеспечивает ЧСС 50-60 в минуту.
Высокоселективный бета1‑блокатор, в отношении которого было доказано снижение смертности от инфаркта миокарда на 32 %. Доза 10 мг бисопролола эквивалентна 100 мг атенолола, препарат назначается в суточной дозировке от 5 до 20 мг. Бисопролол уверенно можно назначать при сочетании гипертонической болезни (снижает артериальную гипертензию), ишемической болезни сердца (уменьшает потребность миокарда в кислороде, уменьшает частоту приступов стенокардии) и сердечной недостаточности (уменьшает постнагрузку).
Метопролол
Препарат относится к бета1‑кардиоселективным бета-блокаторам. У пациентов с ХОБЛ метопролол в дозе до 150 мг/сутки вызывает менее выраженный бронхоспазм по сравнению с эквивалентными дозами неселективных бета-блокаторов. Бронхоспазм при приеме метопролола эффективно купируется бета2‑адреномиметиками.
Метопролол эффективно снижает частоту желудочковых тахикардий при остром инфаркте миокарда и обладает выраженным кардиопротекторным действием, снижая уровень смертности кардиологических больных в рандомизированных исследованиях на 36 %.
В настоящее время бета-адреноблокаторы следует рассматривать как препараты первой линии при лечении ишемической болезни сердца, гипертонической болезни, сердечной недостаточности. Прекрасная сочетаемость бета-блокаторов с мочегонными, блокаторами кальциевых канальцев, ингибиторами АПФ, несомненно, является дополнительным аргументом при их назначении.
Тактика, препараты лечения аллергии гиперчувствительности немедленного типа.
Лечение
аллергических заболеваний следует
начинать с выяснения природы аллергена
(пыльца растений, медикамент, определенная
пища и др.). Устранение контакта с
аллергеном дает наилучший результат.
При
аллергии (гиперчувствительности)
немедленного типа применяют следующие
группы препаратов.
Понижающие
синтез гистамина:
а) глюкокортикоиды
(гидрокортизон, преднизолон, триамцинолон,
дексаметазон);
б) нестероидные
противовоспалительные средства
Препятствующие
освобождению гистамина и других БАВ из
тучных клеток и базофилов:
а) глюкокортикоиды
(гидрокортизон, преднизолон, триамцинолон,
дексаметазон);
б) повышающие
активность аденилатциклазы
— β–адреномиметики
(адреналин, изадрин, орципреналин,
салбутамол, фенотерол), гистаглобулин,
гистамин (малые дозы))
в) ингибиторы
фосфодиэстеразы:
— ксантины
(теофиллин, эуфиллин);
— производные
кромогликата: интал (кромолин-иатрий);
— пиперидина:
кетотифен
г) понижающие
активность гуанилатциклазы
-М-холиноблокаторы
(атропин, атровент)
д) с комбинированным
механизмом действия:
кромоглициевая
кислота (интал);
кетотифен
(задитен);
азеластин
(аллергодил);
лоратадин
(кларитин);
недокромил
натрия (тайлед);
фенспирид
(эреспал);
цитеризин(зиртек)
Увеличивающие
гистаминопексию:
глюкокортикоиды,
гепарин, гистаглобулин, препараты
кальция
Препятствующие
взаимодействию свободного гистамина
с тканевыми рецепторами:
1)
Блокаторы Н1 рецепторов:
а) этаноламины
: дифенгидрамин (димедрол), клемастин
(тавегил), лоредикс (сетастин), цетиризин
(зиртек), левоцетиризин (ксизал)
б) этиленамины:
хлоропирамин (супрастин);
в) фенотиазины:
прометаизин (дипразин);
г) хинуклидины:
хифенадин (фенкарол), бикафен;
д) тетрагидрокарболины:
мебгидролин (диазолин), димебон;
е) пиперидины:
кетотифен, ципрогептадин (перитол),
астемизол, терфенадин (бронал), лоратадин
(кларитин), бамипин (совентол), дезлоратадин
(эриус);
ж) пиперазины
: циннаризин, оксатамид (тимсет), меклозин
(бонин);
з) трипролидина
: акривастин (семпрекс);
другие
фармакологические группы : азеластин
(аллергодил), димебон, диметинден
(фенистил), левокабастин (гистмет),
траниласт, фенспирид (эреспал), эбастин
(кестин);
2) Блокаторы
Н2 рецепторов:
циметидин,
ранитидин, фамотидин, низатидин,
роксатидин
Средства,
уменьшающие повреждение тканей:
глюкокортикоиды.
Средства,
уменьшающие общие проявления аллергических
реакций:
а) адреномиметики;
б) бронхолитики
миотропного действия (эуфиллин);
в) глюкокортикоиды
Описание
Препараты этой группы ингибируют H+-K+-АТФазу (протонный насос) на апикальной мембране париетальных клеток слизистой оболочки желудка. Этот фермент осуществляет перенос ионов водорода из париетальной клетки в просвет желудка.
Высокая селективность ингибиторов протонного насоса обусловлена тем, что их активация возможна только при кислом значении pH (<4). После активации они образуют прочные ковалентные связи с сульфгидрильными группами 813-й аминокислоты (цистеин) H+-K+-АТФазы и тормозят заключительный этап секреции соляной кислоты. Подавление кислотопродукции этими препаратами не зависит от состояния рецепторов (Н2, м3 и др.) на базальной мембране париетальных клеток. Ингибирование протонного насоса омепразолом, лансопразолом, пантопразолом необратимо, рабепразолом — частично обратимо (его комплекс с Н+-К+-АТФазой может диссоциировать).
Ингибиторы протонного насоса дозозависимо подавляют секрецию соляной кислоты, как базальную (ночную и дневную), так и стимулированную (вне зависимости от вида стимула). Эффективно предупреждают усиление секреции после приема пищи. Отмена препарата не сопровождается феноменом рикошета, а кислотопродукция восстанавливается в течение нескольких дней (после синтеза новых молекул H+-K+-АТФазы).
Ингибиторы H+-K+-АТФазы обеспечивают достижение клинико-эндоскопической ремиссии при всех кислотозависимых заболеваниях, в т.ч. требующих пролонгированной или постоянной терапии. Они поддерживают значения рН в желудке в пределах, благоприятных для заживления язвы желудка или двенадцатиперстной кишки длительное время в течение суток. На фоне лечения отмечается быстрое улучшение самочувствия (исчезает болевой синдром и диспептические явления), нормализация морфофункционального состояния слизистой оболочки желудка, сокращение сроков рубцевания пептических язв. Применение при гастроэзофагеальной рефлюксной болезни способствует уменьшению времени экспозиции соляной кислоты в пищеводе, ослаблению повреждающих свойств содержимого желудка. Продолжительность угнетения внутрижелудочной секреции (рН более 4), достигающая 12 ч, обеспечивает возможность заживления эрозивного эзофагита в течение 8 нед.
Ингибиторы протонного насоса увеличивают концентрацию антибактериальных средств в слизистой оболочке желудка и, поддерживая более высокие значения рН, увеличивают активность ряда антибиотиков. Это создает оптимальные условия для проявления эффектов антибактериальных компонентов, входящих в схемы эрадикационной антихеликобактерной терапии (тройная или квадротерапия). Ингибиторы H+-K+-АТФазы обладают и собственным антихеликобактерным эффектом (in vivo подавляют рост Нelicobacter pylory, действуя на систему АТФазы бактерий). Включение ингибиторов H+-K+-АТФазы в комбинированную эрадикационную терапию рекомендуется при язвенной болезни желудка и двенадцатиперстной кишки, ассоциированных с Н. pylori в период обострения и ремиссии, кровоточащей пептической язве, хеликобактерном гастрите с выраженными изменениями слизистой оболочки желудка, мальтомах желудка низкой степени злокачественности, после эндоскопического удаления опухоли желудка. Ингибиторы H+-K+-АТФазы влияют на результаты диагностики инфекции Н. pylori биохимическими методами. Поэтому уреазные тесты для контроля полноты эрадикации Н. pylori могут проводиться не ранее чем через 4 нед после окончания приема.
Ингибиторы протонного насоса предупреждают повреждение слизистой оболочки желудка и двенадцатиперстной кишки НПВС, уменьшают частоту повторных желудочно-кишечных кровотечений (осложнение язвенной болезни), особенно если в процессе лечения была достигнута эрадикация Н. pylori. При хроническом панкреатите способствуют эффективному купированию болевого синдрома за счет подавления секреции и снижения интрапанкреатического давления. Применение ингибиторов протонного насоса может сопровождаться гипергастринемией и повышением уровня пепсиногена I в сыворотке (менее выражены после эрадикации Н. pylori). Через 2–3 нед после прекращения лечения уровень гастрина в сыворотке возвращается к исходному.
Ингибиторы H+-K+-АТФазы могут понижать моторно-эвакуаторную функцию желудка вследствие гипомотилинемии. При длительном применении следует учитывать возможность развития атрофии слизистой оболочки желудка, кампилобактерного гастроэнтерита, чрезмерного размножения и колонизации нехеликобактерных бактерий в слизистой оболочке желудка и тонкой кишки и нарушения динамического равновесия микрофлоры толстой кишки.
История
Создание препаратов этого типа берет свое начало еще в 1972 году, когда английский ученый Джейсм Блек синтезировал и пытался изучить молекулы гистамина. Первый медикамент, который был создан, – Буримамид. Он оказался бесполезным, и исследования продолжились.
После этого структуру немного изменили и получили Метиамид. Исследования по эффективности лекарство прошло, но его токсичность превысила допустимые показатели.

Следующим препаратом стал Циметидин, несмотря на то, что это сильный медикамент, он обладает большим количеством побочных эффектов. Поэтому специалисты разработали более современные лекарства, которые фактически не имеют побочных эффектов.
К второму поколению н2 блокаторов можно отнести Ранитидин. Он получился еще более действенным и безопасным для больных.
Следующим средством этой группы стал Фамотидин. Имеются Блокаторы гистаминовых рецепторов 4 и 5 поколения, но врачи чаще выписывают именно Ранитидин и Фамотидин: они лучше всего справляются с кислотностью в желудочном соке. Принимать Ринитидин можно раз в день, желательно перед сном, препарат хорошо помогает, при этом имеет сравнительно небольшую стоимость.
См. также
- Категория:H1-антигистаминные средства
- Блокаторы H3-гистаминовых рецепторов
Аллерги́я (др.-греч. ἄλλος — другой, иной, чужой + ἔργον — воздействие) — типовой иммунопатологический процесс, выраженный сверхчувствительностью иммунной системы организма при повторных воздействиях аллергена на ранее сенсибилизированный этим аллергеном организм.
Симптомы: резь в глазах, отёки, насморк, крапивница, чихание, кашель и пр.
Антиконгестанты на основе фенилэфрина — комбинированные антиконгестанты, которые содержат адреномиметик фенилэфрин (мезатон), действующий как сосудосуживающее средство. В комбинации с ним используются, как правило, другие сосудосуживающие средства либо антигистаминные препараты (блокаторы H1-гистаминовых рецепторов), действующие как противоаллергические средства.
Они применяются как средства против насморка различного происхождения (ринит при простуде, аллергии, хронический ринит), при синуситах, отитах и в некоторых других случаях (например при подготовке к хирургическому вмешательству в области носа и для устранения послеоперационных отёков слизистой оболочки носа и придаточных пазух).
Ранее вместо фенилэфрина в подобных лекарствах использовался псевдоэфедрин, однако его продажа во многих странах была ограничена, так как он может служить прекурсором для изготовления в кустарных условиях наркотика метамфетамина. Для замены псевдоэфедрина в лекарственных средствах, отпускаемых без рецепта, фармацевтические компании стали использовать схожий с ним по фармакологическому действию фенилэфрин (мезатон).
Буторфанол — лекарственное средство, опиоидный анальгетик.
Гистамин, также имидазолил-2-этиламин — органическое соединение, биогенный амин, медиатор аллергических реакций немедленного типа, также является регулятором многих физиологических процессов.
И́стинная полицитеми́я (от др.-греч. πολυ- — «много» + гистологическое κύτος — «клетка» + αἷμα — кровь) (синонимы: первичная полицитемия, polycythemia vera, эритремия, erythremia, болезнь Вакеза) — доброкачественный опухолевый процесс системы крови, связанный с чрезмерной миелопролиферацией (гиперплазией клеточных элементов костного мозга). Этот процесс в большей степени затрагивает эритробластический росток. В крови появляется избыточное количество эритроцитов, но также увеличивается (в меньшей степени) количество тромбоцитов и нейтрофильных лейкоцитов. Клетки имеют нормальный морфологический вид. За счёт увеличения числа эритроцитов повышается вязкость крови, возрастает масса циркулирующей крови. Это ведёт к замедлению кровотока в сосудах и образованию тромбов, что приводит к нарушению кровоснабжения и гипоксии.
Заболевание впервые было описано Вакезом (Vaquez) в 1892 году. В 1903 году Ослер высказал предположение, что в основе болезни лежит повышенная активность костного мозга. Им же эритремия была выделена в отдельную нозологическую форму.
Истинная полицитемия — болезнь взрослых, чаще лиц пожилого возраста, но встречается и у молодых и детей. Долгие годы болезнь не даёт о себе знать, протекает без симптомов. По разным исследованиям, средний возраст заболевших колеблется от 60 до 70-79 лет. Молодые люди болеют реже, но болезнь у них протекает тяжелее. Мужчины болеют несколько чаще, чем женщины, соотношение приблизительно 1,5:1,0, среди больных молодого и среднего возраста преобладают женщины. Установлена семейная предрасположенность к этому заболеванию, что говорит о генетической предрасположенности. Среди хронических миелопролиферативных заболеваний истинная полицитемия встречается чаще всего. Распространенность составляет 29:100000.
Снотворные средства (от лат. hypnotica; син. гипнотические средства, уст.) — группа психоактивных лекарственных средств, используемых для облегчения наступления сна и обеспечения его достаточной продолжительности, а также при проведении анестезии.
В настоящее время классификация АТС не выделяет такой отдельной фармакологической группы.
Что такое препараты-блокаторы?
Эти препараты разработаны для терапии заболеваний ЖКТ, при которых высокая концентрация соляной кислоты в желудке опасна. Они относятся к лекарственным средствам против язвенной болезни, которые снижают секрецию, т. е. предназначены для уменьшения поступления кислоты в желудок.

Блокаторы группы Н2 имеют различные действующие компоненты:
- циметидин (Гистодил, Альтамет, Циметидин);
- низатидин (Аксид);
- роксатидин (Роксан);
- фамотидин (Гастросидин, Квамател, Ульфамид, Фамотидин);
- ранитидин (Гистак, Зантак, Ринисан, Ранитиддин);
- ранитидина висмута цитрат (Пилорид).
Средства выпускают в виде:
- готовых растворов для внутривенного или внутримышечного введения;
- порошка для приготовления раствора;
- таблеток.
На сегодняшний день циметидин не рекомендован к применению из-за большого количества побочных эффектов, включающих снижение потенции и увеличение грудных желез у мужчин, развитие болей в суставах и мышцах, повышение уровня креатинина, изменения в составе крови, поражение ЦНС и др.
Ранитидин имеет гораздо меньше побочных действий, но его все реже применяют в медицинской практике, так как на смену приходят препараты следующего поколения (Фамотидин), чья эффективность намного выше, а время действия на несколько часов дольше (от 12 до 24 часов).
В каких случаях назначают блокаторы?
Увеличение уровня кислоты в желудочном соке опасно при:
- язве желудка или двенадцатиперстной кишки;
- воспалении пищевода при забрасывании содержимого желудка в пищевод;
- доброкачественной опухоли поджелудочной в комплексе с язвой желудка;
- приеме для профилактики развития язвенной болезни при длительной терапии других заболеваний.
Конкретный препарат, дозы и длительность курса подбираются индивидуально. Отмена лекарства должна происходить постепенно, так как при резком окончании приема возможны побочные эффекты.
Недостатки в работе блокаторов гистамина
Блокаторы Н2 влияют на выработку свободного гистамина, снижая тем самым кислотность желудка. Но эти препараты не действуют на другие стимуляторы синтеза кислоты – гастрин и ацетилхолин, то есть полного контроля над уровнем соляной кислоты эти лекарства не дают. Это одна из причин того, что медики считают их относительно устаревшими средствами. Тем не менее есть ситуации, когда оправдано назначение именно блокаторов.
Существует довольно серьезный побочный эффект терапии с использованием блокаторов Н2 гистаминовых рецепторов – так называемый «кислотный рикошет». Он заключается в том, что после отмены препарата или окончания его действия желудок стремится «наверстать упущенное», и его клетки увеличивают выработку соляной кислоты. В результате через некоторый промежуток после принятия лекарства кислотность желудка начинает повышаться, вызывая обострение болезни.
Еще одно побочное действие – диарея, вызванная патогенным микроорганизмом клостридия. Если совместно с блокатором больной принимает антибиотики, то риск появления диареи увеличивается в десятки раз.
Как ведут себя в организме
- Препараты этой группы, как правило, хорошо всасываются в начальном отделе тонкой кишки.
- Функция Н2-гистаминоблокаторов незначительно снижается при одновременном приеме с антацидами и сукральфатом.
- Цели в организме (то есть, собственно обкладочных клеток) достигает не вся доза принятого внутрь препарата, а лишь его часть (в фармакологии этот показатель называют биодоступностью). У циметидина биодоступность составляет 60-80 %, ранитидина – 55-60 %, фамотидина – 30-50 %, роксатидина – более 90 %. Если Н2-гистаминоблокатор вводится внутривенно, его биодоступность стремится к 100 %.
- После приема внутрь максимальная концентрация препарата в крови определяется через 1-3 часа.
- Проходят через печень, претерпевая в ней ряд химических изменений, выводятся с мочой.
- Период полувыведения ранитидина, циметидина и низатидина составляет 2 часа, фамотидина – 3.5 часа.
Механизм действия Н2-блокаторов и показания к применению
На мембране внутри стенки желудка расположены гистаминовые (Н2) клеточные рецепторы. Это париетальные клетки, которые в организме причастны к выработке соляной кислоты.
Ее чрезмерная концентрация вызывает нарушения в функционировании пищеварительной системы и приводит к язве.
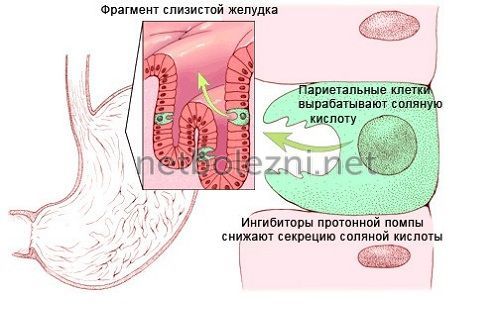
Вещества, которые содержатся в Н2-блокаторах
, имеют свойство снижать уровень выработки желудочного сока. Также они угнетают уже готовую кислоту, выработка которой спровоцирована потреблением пищи.
В связи с оказываемым действием, Н2-блокаторы назначают при таких состояниях:
- язва (как желудка, так и двенадцатиперстной кишки);
- стрессовая язва — вызванная тяжелыми соматическими заболеваниями;
- язва, возникшая на фоне длительного приема нестероидных противовоспалительных или кортикостероидных препаратов;
- острый панкреатит и обострение хронического;
- в сочетании с ферментными панкреатическими препаратами, с целью их защиты от разрушающего воздействия желудочного сока.
Дозировка и длительность приема Н2-антигистаминных лекарственных препаратов при каждом из перечисленных диагнозов назначается индивидуально.
Описание
Первые лекарственные средства, блокирующие Н1-гистаминовые рецепторы, были внедрены в клиническую практику в конце 40-х годов. Они получили название антигистаминных, т.к. эффективно ингибируют реакции органов и тканей на гистамин. Блокаторы гистаминовых Н1-рецепторов ослабляют вызываемые гистамином гипотензию и спазмы гладкой мускулатуры (бронхов, кишечника, матки), уменьшают проницаемость капилляров, препятствуют развитию гистаминового отека, уменьшают гиперемию и зуд и, таким образом, предупреждают развитие и облегчают течение аллергических реакций. Термин «антигистаминные» неполностью отражает спектр фармакологических свойств этих препаратов, т.к. они вызывают и ряд других эффектов. Частично это обусловлено структурным сходством гистамина и других физиологически активных веществ, таких как адреналин, серотонин, ацетилхолин, дофамин. Поэтому блокаторы гистаминовых H1-рецепторов могут в той или иной степени проявлять свойства холинолитиков или альфа-адреноблокаторов (холинолитики, в свою очередь, могут обладать антигистаминной активностью). Некоторые антигистаминные средства (дифенгидрамин, прометазин, хлоропирамин и др.) оказывают угнетающее влияние на ЦНС, усиливают действие общих и местных анестетиков, наркотических анальгетиков. Они применяются при лечении бессонницы, паркинсонизма, в качестве противорвотных средств. Сопутствующие фармакологические эффекты могут быть и нежелательными. Например, седативное действие, сопровождающееся вялостью, головокружением, нарушением координации движений и понижением концентрации внимания, ограничивает амбулаторное использование некоторых антигистаминных препаратов (дифенгидрамин, хлоропирамин и другие представители I поколения), особенно у пациентов, работа которых требует быстрой и координированной умственной и физической реакции. Наличие у большинства из этих средств холинолитического действия обусловливает сухость слизистых оболочек, предрасполагает к ухудшению зрения и мочеиспускания, дисфункции ЖКТ.
Препараты I поколения являются обратимыми конкурентными антагонистами Н1-гистаминовых рецепторов. Они действуют быстро и коротко (назначаются до 4 раз в сутки). Их длительное использование часто приводит к ослаблению терапевтической эффективности.
Позже были созданы блокаторы гистаминовых H1-рецепторов (антигистаминные препараты II и III поколения), отличающиеся высокой избирательностью действия на Н1-рецепторы (в т.ч. хифенадин, терфенадин, астемизол, лоратадин, эбастин). В настоящее время в ряде стран (в т.ч. и в России) терфенадин и астемизол изъяты из обращения в связи с кардиотоксичностью (удлинение интервала QT). Препараты II поколения незначительно влияют на другие медиаторные системы (холинергические и др.), не проходят через ГЭБ (не влияют на ЦНС) и не теряют активность при длительном применении. Многие препараты II поколения неконкурентно связываются с Н1-рецепторами, а образовавшийся лиганд-рецепторный комплекс характеризуется сравнительно медленной диссоциацией, обусловливающей увеличение продолжительности терапевтического действия (назначаются 1 раз в сутки). Биотрансформация большинства антагонистов гистаминовых Н1-рецепторов происходит в печени с образованием активных метаболитов. Ряд блокаторов Н1-гистаминовых рецепторов представляет собой активные метаболиты известных антигистаминных препаратов (цетиризин — активный метаболит гидроксизина, фексофенадин — терфенадина, дезлоратадин — лоратадина).
Поколения Н2-блокаторов[править | править код]
Принята следующая классификация Н2-блокаторов по поколениям:
- I поколение — циметидин,
- II поколение — ранитидин,
- III поколение — фамотидин,
- IV поколение — низатидин,
- V поколение — роксатидин.
Циметидин, Н2-блокатор I поколения, обладает серьёзными побочными проявленими: он блокирует периферические рецепторы мужских половых гормонов (андрогенные рецепторы), существенно снижая потенцию и приводит к развитию импотенции и гинекомастии. Также возможны диарея, головные боли, транзиторные артралгии и миалгии, блокирование системы цитохрома Р450, повышение уровня креатинина в крови, поражение центральной нервной системы, гематологические изменения, кардиотоксические эффекты, иммуносупрессивное действие.
Ранитидин имеет меньше типичных для циметидина побочных эффектов, а препараты последующих поколений — ещё меньше. При этом активность фамотидина в 20—60 раз превышает активность циметидина и в 3-20 раз активность ранитидина. По сравнению с ранитидином фамотидин более эффективно повышает рН и снижает объем желудочного содержимого. Длительность антисекреторного действия ранитидина — 8-10 часов, а фамотидина — 12 часов.
Н2-блокаторы IV и V поколений низатидин и роксатидин на практике мало чем отличаются от фамотидина и не имеют перед ним существенных преимуществ, а роксатидин даже немного проигрывает фамотидину в кислотоподавляющей активности.