Mycobacterium tuberculosis
Содержание:
Антигены
Микобактерии имеют специфические видовые и межвидовые и даже межродовые антигенные связи. В отдельных штаммах выявлены различные антигены. Однако все без исключения микобактерии содержат вещества, устойчивые к нагреванию и воздействию протеолитических ферментов — полисахариды, которые являются общим антигеном.
Кроме того, различные виды микобактерий имеют свои специфические антигены. А. П. Лысенко (1987) доказал, что все штаммы M. bovis имеют идентичный антигенный спектр с 8 антигенов, из которых 5-6 были общеродовыми и реагировали с антисыворотками к микобактерий других видов: 6 — с M. tuberculosis, 3-5 — M. kansasii и т.д.
Виды лекарственной устойчивости
Первичная медикаментозная устойчивость — устойчивость, обнаруженная у впервые выявленных больных, которые никогда не принимали противотуберкулезные препараты.
Начальная медикаментозная устойчивость — устойчивость МБТ, выявленная у впервые выявленных больных, леченных противотуберкулезными препаратами не более 4 недель или у больных при отсутствии данных о предшествующем лечении. Вторичная (приобретенная) медикаментозная устойчивость — резистентность МБТ, обнаружена у больных, которым назначали противотуберкулезные препараты более 4 недели. Монорезистентность — устойчивость МБТ против 1 из 5 препаратов I ряда (изониазиду стрептомицина, рифампицина, этамбутола, пиразинамида).
В Украине частота возникновения первичной резистентности возбудителя туберкулеза против препаратов I ряда отмечается в 23-25%, а вторичной — в 55-56% случаев. Множественная лекарственная устойчивость — устойчивость МБТ против двух и больше препаратов. Мультирезистентность — это разновидность множественной лекарственной устойчивости, и именно — устойчивость возбудителя только против комбинации изониазид + рифампицин или и рядом: другими препаратами.
Результат определения чувствительности микобактерий туберкулеза к противотуберкулезным препаратам называется антибиограмой.
Причины лекарственной устойчивости:
1. Биологические — недостаточная концентрация препарата, индивидуальные особенности организма пациента (скорость инактивации препаратов)
2. Причины, обусловленные пациентом — контакт с больными химиорезистентным туберкулез, нерегулярный прием препаратов, преждевременное прекращение приема лекарств, неудовлетворительная переносимость препаратов, проведение неадекватного лечения.
3. Факторы, обусловленные болезнью — при изменении доз препаратов, при большом количестве МБТ в участках пораженного органа может возникать определенная рН, которая препятствует активному действию лекарств, лечение одним препаратом, недостаточная доза или продолжительность лечения.
Пути заражения туберкулезом
Основными путями проникновения микобактерий туберкулеза в организм человека или животного являются:
- аэрогенный (воздушно-капельный и пылевой),
- алиментарный,
- контактный,
- внутриутробний.
Аэрогенный путь
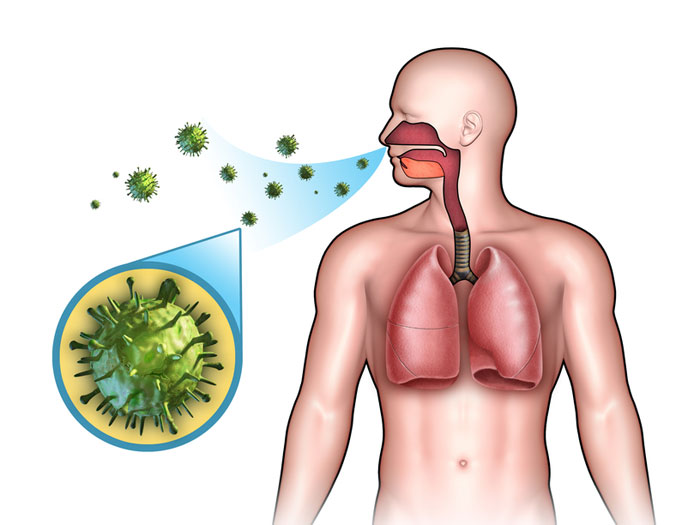
Аэрогенный путь заражения является основным (95-97% случаев). При кашле и разговоры больной туберкулезом выделяет капли слюны и мокроты. Эти капли распространяются на 1,5-2 м и находятся в воздухе 1-1,5 ч., а затем оседают на пол. Такой путь распространения микобактерий и заражения называется воздушно-капельным. При большом скоплении людей (очереди, общественный транспорт, рынок и другие места), а также при внутрисемейном общении этот путь заражения особенно опасен.
Капли мокроты, что высохли и осели на пол, превращаются в пыль. Заражение возможно при непосредственном вдыхании пыли (пылевой путь), содержащий микобактерии туберкулеза. В пыли, который взят из помещения, где находился больной туберкулезом, микобактерии оказываются в 30% случаев, иногда даже через 1,5 мес. Но при соблюдении правил гигиены (обеззараживания мокроты, уборка помещения) воздуха, даже туберкулезных диспансеров, не содержит микобактерий туберкулеза.
При дыхании большая часть капелек и пыли оседает на слизистой оболочке носа миндалинах, зеве. Поэтому возможно проникновение микобактерий туберкулеза через слизистую оболочку зева и возникновения лимфаденита шеи. Затем возбудитель попадает во внутригрудные лимфатические узлы, лимфатический грудной проток и кровь.
Неповрежденная слизистая оболочка трахеи и бронхов является барьером на пути проникновения микобактерий туберкулеза, но в случае травмы или воспаление слизистой оболочки они могут проникать в пределах трахеи и бронхов. Однако в большинстве случаев проникновения микобактерий туберкулеза во внутреннюю среду организма происходит в альвеолах при условии нарушения местного иммунитета.
Алиментарный путь
Алиментарный путь проникновения инфекции наблюдается в случаях употребления пищевых продуктов, полученных от больных туберкулезом животных, а также инфицирование пищи, посуды и других предметов. При этом возбудитель туберкулеза заглатывается и проникает с пищей или слюной в желудок, а затем в тонкий кишечник, откуда с током лимфы и крови заносится в лимфатические сосуды, лимфатические узлы и кровь. Возможность алиментарного пути проникновения туберкулезной инфекции убедительно доказана любекской трагедией, когда из-за преступной халатности врачей 250 детям вместо вакцины был дан вирулентный килльський штамм МБТ. Вследствие этого 2/3 детей заболели и 1/2 умерли от генерализованной формы туберкулеза.
Чаще алиментарным путем люди заражаются при употреблении молока от коров больных туберкулезом. Мясо и яйца животных, больных туберкулезом, имеют меньшее эпидемиологическое значение, так как их почти всегда перед употреблением подвергают термической обработке, и в них концентрация МБТ незначительна.
Контактный путь
Контактный путь проникновения туберкулезной инфекции может наблюдаться у хирургов, патологоанатомов, мясников, лаборантов, доярок, когда возбудитель туберкулеза попадает непосредственно через поврежденную кожу или конъюнктиву. Следовательно, входной воротами туберкулезной инфекции являются дыхательные пути и пищеварительный канал, поврежденная кожа, миндалины и конъюнктива.
Внутриутробний путь
Возможен также внутриутробний путь передачи туберкулезной инфекции. Как правило, женщины даже с активными формами туберкулеза рожают доношенных здоровых детей. Если сразу после родов этих детей изолировать от матерей, а затем вакцинировать и создать соответствующие гигиенично диетические условия для их развития, то дети вырастают здоровыми и не болеют туберкулезом.
Поврежденная плацента является барьером на пути проникновения туберкулезной инфекции: крови матери в кровь плода. Поэтому внутриутробная инфекция возможна при генерализованных формах процесса и появлению туберкулезных бугорков на плаценте, а также в случаях родовой травмы, когда происходит смешивание крови плода и матери.
На протяжении веков человечество сталкивалось с туберкулезной инфекцией, которая «обитает» в окружающей среде. При этом 80-90% людей заразились и имели следы этой инфекции в легких. Естественно, что в организме человека производились механизмы защиты в микобактерий туберкулеза. Так как это продолжалось из поколения в поколение, то в конце концов люди унаследовали естественную резистентность к туберкулезу.
Что такое туберкулез?
Туберкулез – это заразное инфекционное заболевание, основной причиной которого является инфицирование организма палочками Коха (Mycobacterium tuberculosis complex). Основные симптомы туберкулеза, при его классическом течении – кашель с мокротой (часто с примесью крови), слабость, лихорадка, значительная потеря веса, ночная потливость и другие.
Самый главный очаг поражения – дыхательные пути (бронхи легкие), но иногда микобактерии вызывают воспаление в лимфатической, нервной и мочеполовой системе, опорно-двигательном аппарате, на коже, или даже поражают весь организм целиком (милиарная форма).
Возбудителем туберкулёза является микобактерия (Mycobacterium tuberculosis). Наиболее распространённый путь передачи туберкулёза — воздушно-капельный. Туберкулёзная палочка при этом передаётся при контакте во время разговора, чихания, пения или кашля, а также через предметы обихода.
Иммунная система здорового человека справляется с инфекцией, уничтожив палочку Коха в дыхательных путях. Слишком массивная инфекция или частый контакт с больным может вызвать заболевание даже у здорового человека. У людей с ослабленной иммунной системой её клетки не в состоянии разрушить микобактерии.
Особенности микобактерии:
- Высокая устойчивость к кислотам, спиртам, щелочам
- Быстрее размножается и предпочитает тёмные, невентилируемые, влажные помещения
- Устойчивость к холоду
- Прямые солнечные лучи, тепло не переносит
- Хлорсодержащие вещества являются губительными.
Инкубационный период туберкулеза, т.е. период, от момента попадания палочки Коха до появления первых признаков заболевания, составляет от 2 до 12 недель, в среднем – 6-8 недель, иногда год и более.
Иммунные реакции (ПЗЧТ)
Когда Mycobacterium tuberculosis проникает в альвеолы легких, они взаимодействуют с макрофагами. Иммунные клетки сначала фиксируют патоген на своей мембране, а затем поглощают его. Внутри происходит активный синтез ферментов, направленных на разрушение антигена.
Если вышеперечисленные действия безуспешны, бактерия остается жизнеспособной, размножается и уничтожает сам макрофаг. В окружающее пространство помимо палочек Коха выделяются биологические вещества.активный, развивается воспаление. Сначала начинается процесс экссудации с нарушения кровоснабжения, затем следует изменение (туберкулезная гранулема). Последний отвечает за иммунную реакцию на клеточном фоне — гиперчувствительность замедленного типа (DHS, DHP).
TDRH при туберкулезе — это тип аллергии, который включает взаимодействие антигена (микобактерии) с макрофагами и Т-лимфоцитами. В этот момент вырабатывается интерлейкин-1 (медиатор воспаления), который увеличивает активность CD4 + клеток (клеток-помощников, тип лимфоцитов). Усиливается процесс фиброза, что приводит к обратному развитию патологического процесса. Таким образом, при туберкулезе специфический иммунитет и аллергия тесно связаны.
Геном микобактерий туберкулеза
В последние годы интенсивно проводили генетические исследования штамма М. tuberculosis. Количество гуанинцитозиновых основ, которые распределяются на спирали дезоксирибонуклеиновой кислоты (ДНК), составляет 65,5%. Геном содержит много вставных последовательностей, мультигенных семей, амплифицированных (удвоенных) мест собственного обмена веществ.
РНК-молекулы кодируют около 50 генов, в частности:
- три вида рибосомных РНК, которые синтезируются из уникального рибосомного оперона;
- гены, кодирующие 108-РНК, включается в процесс разрушения белков (выявлено, что эти 108-РНК кодируются так называемыми ненормальными и РНК-мессенджерами);
- гены, кодирующие РНК-компонентную РНКазу Р;
- гены транспортных РНК.
М. tuberculosis имеет 11 рецепторзависимых гистидинкиназ, несколько цитоплазматических киназ и немного генов, участвующих в регуляторных каскадах. В М. tuberculosis является группа эукариотических серинтиреонинових протеинкиназ, отвечающих за фосфорилирование в бактериальной клетке.
1. РабА / РабВ-Р-оксидазные комплексы.
2. Тридцать шесть ацил-СоА-синтетаз и группа из тридцати шести ацил-СоА-синтетазсвязанных белков.
3. Пять ферментов, завершают цикл окисления (реакция тиолиза 3 кетоэстеров).
4. Четыре гидроксиацил-СоА-дегидрогеназы.
5. Двадцать один вид белков эноил-СоА-гидратазо-изомеразной группы.
6. Ацетил-СоА-С-ацетилтрансферазы.
Патогенность М. tuberculosis обусловлена также такими факторами, как: 1) антиоксидазная каталазная-пероксидазная система;
2) сигма-фактор;
3) МСЭ-оперон, кодирующий белки внутриклеточной инвазии;
4) фосфолипаза С;
5) ферменты, продуцирующие компоненты клеточной стенки;
6) гематоглобиноподобные Ре-связующие белки, которые обеспечивают длительное анаэробное существование микобактерий;
7) эстеразы и липазы;
8) значительная антигенная лабильность;
9) наличие различных путей обеспечения антибиотикорезистентности;
10) наличие актериоцинов с цитотоксическим действием (некоторые поликетины).
Хронический диссеминированный туберкулез легких
Возникает чаще всего вследствие острого или подострого диссеминированного туберкулеза легких. Характерным признаком является наличие очагов различной интенсивности и размеров среди фиброзно измененной легочной ткани. Если очаги локализуются в верхних отделах легких, то это ограниченная форма, а если поражаются все отделы легких, то это распространенная форма.
Симптомы
Хронический диссеминированный туберкулез легких имеет волнообразное течение, при котором симптомы в период ремиссии частично угасают, а при обострении процесса — усиливаются. Эта форма туберкулеза сопровождается мало выраженными признаками интоксикации. Часто больные чувствуют себя удовлетворительно. При тщательном расспросе жалуются на общую слабость, одышку при физической нагрузке.
Выделение МБТ возникает при распаде легочной ткани и образовании каверны. Когда происходит прогрессирование процесса с образованием деструктивных изменений в легких, нарастают симптомы интоксикации, может возникать кровохарканье. Одновременно появляются признаки хронического легочного сердца — одышка, диффузный цианоз.
Вследствие развития фиброза у больных хроническим диссеминированным туберкулезом легких в верхних отделах нередко образуются бронхоэктазы, поэтому перкуторно определяется укорочение легочного звука. В нижних отделах развивается эмфизема, поэтому здесь определяется тимпанит. В легких, чаще в паравертебральной области, выслушиваются сухие, реже — влажные хрипы.
Изменения в анализе крови характеризуются:
- незначительным лейкоцитозом,
- сдвигом лейкоцитарной формулы влево,
- моноцитозом,
- повышением СОЭ.
При стабилизации процесса анализ крови может быть не измененным.
Рентгенологическими признаками хронического диссеминированного туберкулеза легких являются:
— Асимметрично размещенные полиморфные очаги (разных размеров и плотности) — симптом «звездного неба». Большие плотные очаги отмечаются в верхних долях легких;
— Наличие «штампованных каверн»;
— Фиброзные изменения в легких (симптом «плакучей ивы»);
— Бронхоэктазы, эмфизема, эмфизематозные были.
Последствия. Благоприятные — уплотнения и петрификация очагов. Относительно благоприятные — развитие фиброзных изменений, эмфиземы, бронхоэктазов. Неблагоприятные — переход в фиброзно-кавернозный туберкулез легких или казеозную пневмонию.
Дифференциальная диагностика диссеминированного туберкулеза проводится с:
- двусторонней очаговой пневмонией,
- бронхиолитом,
- карциноматозом легких,
- пневмокониозами (силикозом и т.п.),
- саркоидозом,
- застойными явлениями в легких,
- коллагенозаным муковисцидозом.
ПУТИ И МЕХАНИЗМЫ ПЕРЕДАЧИ ИНФЕКЦИИ
Механизм передачи инфекции — совокупность эволю- ционно сложившихся способов перемещения возбудителя инфекционной (паразитарной) болезни от источника в восприимчивый организм.
Путь передачи возбудителя — совокупность факторов, обеспечивающих проникновение возбудителя в восприимчивый организм в конкретных условиях места и времени.
Один механизм может реализоваться различными путями, например: фекально-оральному механизму соответствуют контактно-бытовой, пищевой и водный пути; аэрозольно-аэрогенному — воздушно-капельный и воздушно-пылевой; гемоконтактному — парентеральный, трансплантационный, вертикальный и половой.
1. Фекально-оральный механизм осуществляется при непосредственном общении (прямой контакт) или через зараженные предметы окружающей среды (непрямой контакт).
•
Контактно-бытовой путь — через предметы домашнего обихода (полотенце, белье, игрушки, посуду); часто осуществляется при шигеллезе.
•
Пищевой путь — через молоко и молочные продукты, мясо, яйца, рыбу, загрязненные овощи, фрукты и пр.; является основным при шигеллезе, сальмонеллезе, кишечных инфекциях.
•
Водный путь: брюшной тиф и паратифы, шигеллез (шигеллы Флекснера), туляремия, лептоспироз, вирусный гепатит ,4 (ВП4), холера.
2.
Аэрозольно-аэрогенный механизм
•
Воздушно-капельный путь — проникновение с воздухом капель инфицированной слизи и слюны, выделенной при кашле, чихании и разговоре, таким способом передаются корь, ветряная оспа, грипп и др.
•
Воздушно-пылевой путь — в организм человека с воздухом попадают частицы взвешенной пыли, содержащей инфекционный агент (при дифтерии, скарлатине и др.).
3.
Трансмиссивный механизм осуществляется посредством переносчиков, являющихся чаще всего биологическими хозяевами возбудителей и реже — механическими переносчиками. Переносчиков делят на две группы:
1)
специфические блохи — чума, вши — сыпной тиф, комары — малярия, москиты — лихорадка паппатачи, лейшманиоз, клещи — арбовирусные энцефалиты, возвратный тиф и др.;
2)
неспецифические (мухи — острые кишечные инфекции, гепатит Л, брюшной тиф и паратифы).
4.
Гемоконтактный механизм
•
Вертикальный (трансплацентарный, внутриутробный) путь — передача возбудителя болезни через плаценту (вертикально) от матери к плоду; доказана возможность передачи вирусов краснухи, кори, ветряной оспы, эпидемического паротита, гепатита В, цитоме- галовируса (ЦМВ), энтеровирусов, вируса иммунодефицита человека (ВИЧ), возбудителей листериоза, лептоспироза и т.д.
•
Парентеральный путь реализуется при проведении медицинских манипуляций, при которых возможен контакт инструментов с кровью (вирусы гепатита В, С, ВИЧ и др.).
•
Трансплантационный путь реализуется при трансплантации органов (вирусы гепатита В, С, ВИЧ и др.).
•
Половой путь реализуется при половых контактах (заболевания, передающиеся половым путем, ВИЧ, вирус гепатита В и др.).
предыдущая
к содержанию
следующая
А так же в разделе «2. ПУТИ И МЕХАНИЗМЫ ПЕРЕДАЧИ ИНФЕКЦИИ »
- 1.ПОНЯТИЯ «ИНФЕКЦИЯ», «ИНФЕКЦИОННЫЙ ПРОЦЕСС»,«ИНФЕКЦИОННАЯ БОЛЕЗНЬ». ХАРАКТЕРИСТИКА ВОЗБУДИТЕЛЕЙ
- 3. РЕЗИСТЕНТНОСТЬ МАКРООРГАНИЗМА.СТАДИИ РАЗВИТИЯ ИНФЕКЦИОННОЙ БОЛЕЗНИ
- 4. КЛАССИФИКАЦИЯ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ
- 5. ВНУТРИБОЛЬНИЧНЫЕ ИНФЕКЦИИ
Коллагенозы
Под этим названием объединены ряд заболеваний, характеризующихся диффузным поражением соединительной ткани и сосудов (ревматизм, ревматоидный артрит, системная красная волчанка, узелковый периартериит, системная склеродермия, дерматомиозит). При этих заболеваниях возникают изменения в легких, которые иногда ошибочно принимают за диссеминированный туберкулез.
Собственно колагенозные поражения в легких при различных нозологических формах неодинаковы и могут проявляться очагами, инфильтратами, четко очерченными узлами, тонкостенными пустотами, полосатыми тенями, усилением и деформацией легочного рисунка, плевральными изменениями. Можно обнаружить также двустороннюю диссеминацию и плевральный выпот, что характерно для диссеминированного туберкулеза легких, от которого нужно их дифференцировать.
Сходство проявляется и в общих клинических симптомах (лихорадка, снижение массы тела, боль в груди, кашель с мокротой, иногда кровохарканье, одышка, цианоз, хрипы в легких) и в рентгенологической картине в легких. К ним относятся: очаговые изменения, полостные образования, плеврит.
Диагностические критерии коллагенозов:
- коллагенозам свойственно формирование васкулитов (сопровождающиеся кровохарканьем, одышкой) и периваскулярного склероза рентгенологически проявляется усилением легочного рисунка и очаговоподобными тенями, которые напоминают диссеминированный туберкулез легких;
- для коллагенозов характерно одновременное поражение многих органов: кожи, суставов, почек, легких, лимфатических узлов, плевры, сердца и других;
- коллагенозы имеют ряд особенностей, которые присущи отдельным видам коллагенозов;
- характерные аллергические и аутоиммунные реакции в виде кожных высыпаний, артритов, артралгий;
- в крови обнаруживают высокое содержание фибриногена, Р- и у-глобулинов, значительное повышение СОЭ;
- часто может возникать астматический компонент заболевания, быстро проходит;
- рентгенологические проявления этих заболеваний характеризуются двусторонним симметричным поражением; однако локализация диссеминированного туберкулеза — преимущественно в верхних и средних отделах легких, а колагенозные изменения — в нижних и прикорневых;
- вовлечение в процесс плевры (плеврит) свойственно обоих заболеваний, но при туберкулезе оно чаще одностороннее, при коллагенозах — двустороннее и плеврит имеет склонность к быстрому исчезновению (ревматизм, ревматоидный артрит, системная красная волчанка, узелковый периартериит);
- формирование полостей распада при туберкулезе сопровождается бактериовыделением, при коллагенозах возможно возникновение тонкостенных полостей, но МБТ не находят.
- Для дифференциальной диагностики этой группы заболеваний следует использовать бронхоскопию, проводить биопсию кожи, мышц.
Свежее колагенозное поражение легких, в отличие от туберкулеза, быстро проходит на фоне кортикостероидной терапии, оставляя после себя фиброзные и буллезно-дистрофические изменения. Лечение туберкулеза длительное, обратное развитие медленное.
В процессе обследования больных колагенозом с синдромом легочной диссеминации нужно учитывать возможность присоединения туберкулеза под влиянием массивной кортикостероидов, поэтому нужно детальное клинико-рентгенологическое обследование больного, туберкулинодиагностика, многократные поиски МБТ.
Типы микобактериоза
Различают три типа микобактериоза, которые зависят от вида микобактерий и иммунного статуса организма:
1. Генерализованная инфекция с развитием видимых невооруженным глазом патологических изменений внешне напоминают туберкулезные, но гистологически несколько отличаются от них. В легких обнаруживают диффузные интерстициальные изменения без гранулем и полостей распада. Основными признаками являются повышение температуры тела, двусторонняя диссеминация в средних и нижних отделах легких, анемия, нейтропения, хроническая диарея и боль в животе. Диагноз подтверждается нахождением возбудителя в мокроте, кале или биопсией. Эффективность лечения низкая, смертность высокая и достигает 20%. Эффективными для лечения при микобактериоза является циклосерин, этамбутол, канамицин, рифампицин и частично стрептомицин.
2. Локализованная инфекция — характеризуется наличием макро- и микроскопических поражений, выявляемых в определенных участках тела.
3. Инфекция, которая протекает без развития видимых поражений; возбудитель находится в лимфатических узлах.
Туберкулез у людей преимущественно (95-97%) возникает вследствие заражения человеческим, реже (3-5%) бычьим и казуистически — птичьим видом микобактерий туберкулеза. М. africanum вызывает туберкулез у людей в странах Тропической Африки.
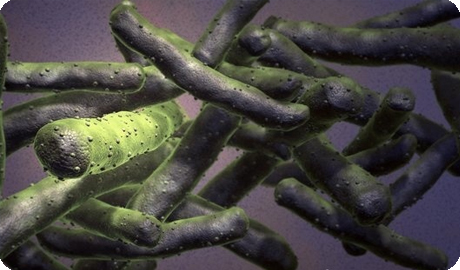
М. tuberculosis
Микобактерии туберкулеза имеют форму тонких, длинных или коротких, прямых или искривленных палочек, длиной 1,0-4,0 мкм и диаметром 0,3-0,6 мкм; неподвижные, спор и капсул не образуют, грамположительные, имеют большой полиморфизм.
Микобактерии туберкулеза человеческого вида более тонкие и длинные, чем бычьего. Микобактерии бычьего вида менее патогенны для людей, и заболевание, вызванное ими, встречается значительно реже. Для определения МБТ человеческого вида применяют ниациновий тест. Он базируется т том, что МБТ этого вида выделяют больше ниацина (никотиновой кислоты).
Молодые бактерии гомогенные, в процессе их старения образуется зернистость (зерна Муха), которая более подробно изучается методом электронной микроскопии. Зернистая форма микобактерий туберкулеза образуется также под влиянием антимикобактериальных препаратов. После введения зерен животным у них возникает кахексия, увеличение лимфатических узлов или заболевания туберкулезом с развитием типичных штаммов микобактерий туберкулеза. Описанные оскольчатые формы микобактерий туберкулеза. Возбудитель туберкулеза может существовать также в виде фильтрующихся форм.
Под влиянием противотуберкулезных препаратов морфологические и физико-химические свойства микобактерий туберкулеза изменяются. Микобактерии становятся короткими, приближаясь к кокобацилам, их кислотостойкость уменьшается, поэтому при окраске по Цил-Нильсену они обесцвечиваются и не определяются.
Туберкулез неустановленной локализации
Туберкулез неустановленной локализации — это так называемая «туберкулезная интоксикация» у детей. Туберкулезная интоксикация как отдельная форма туберкулеза — это симптомокомплекс функциональных расстройств, обусловленный первичным проникновением МБТ в организм.
Эта форма туберкулеза не диагностируется рентгенологически и инструментальными методами исследования. При наличии признаков туберкулезной интоксикации нужно сделать обзорную рентгенограмму и срединную томограмму. В случае выявления увеличенных лимфатических узлов ставят диагноз форме туберкулеза внутригрудных лимфатических узлов.
Патоморфология. При туберкулезной интоксикации в лимфатических узлах развиваются гистиомакрофагальные бугорки. Позже появляются эпителиоидные и гигантские клетки Пирогова-Лангханса, лимфоциты и макрофаги.
Симптомы. Для туберкулезной интоксикации основным признаком является интоксикационный синдром, появляется в период или сразу после виража туберкулиновой пробы. Наиболее характерны изменения поведения ребенка — он становится раздражительным или заторможенной, быстро устает, появляются субфебрильная температура, головная боль, ухудшение аппетита и сна, увеличиваются периферические лимфатические узлы (микрополиаденит). Температура тела не имеет постоянного характера, отмечаются ее колебания в течение суток.
Со стороны крови отмечается лимфоцитоз, сдвиг лейкоцитарной формулы влево.
Диагностика туберкулезной интоксикации основывается на следующих данных:
• Наличие синдрома интоксикации.
• Появление виража туберкулиновой пробы диаметром инфильтрата более 12 мм.
• Микрополиаденит, чаще в области заднего треугольника шеи.
• Обременительная наследственность.
• Наличие контакта с больным туберкулезом, особенно с бактериовыделителем.
• Проведение дифференциальной диагностики с заболеваниями, которые имеют сходные симптомы интоксикации.
• Наличие и выраженность поствакцинального рубчика.
• В случае необходимости применяют тест-терапию антимикобактериальными препаратами узкого спектра действия.
Если в результате лечения наступает улучшение, исчезают клинические проявления, то ЦС свидетельствует в пользу диагноза туберкулезной интоксикации.
Лечение. Детей и подростков с туберкулезной интоксикацией лечат в стационаре. Назначают ежедневно изониазид с этамбутолом или пиразинамидом. Следует отметить, что туберкулезная интоксикация — единственная форма туберкулеза, которую можно лечить одним изониазидом, но лучше назначать его в сочетании с другими препаратами. Лечение проводят в течение 3-4 месяцев до стойкого исчезновения симптомов интоксикации.
Последствия. Благоприятный исход — выздоровление больного. Возможно также и спонтанное выздоровление Неблагоприятный исход — переход туберкулезной интоксикации в локальную форму первичного туберкулеза.
Дифференциальная диагностика туберкулезной интоксикации проводится с:
- хроническим тонзиллитом,
- ревматизмом, синуситами,
- пиелонефритом,
- гипертиреозом,
- гепатохолециститом,
- глистной инвазией,
- хроническими неспецифическими воспалительными заболеваниями легких.
Диагностика туберкулезной интоксикации как клинической формы первичного туберкулеза неустановленной локализации иногда бывает сложная. Развивается туберкулезная интоксикация на фоне виража туберкулиновых реакций или вскоре после его установки. Поэтому при опросе ребенка и его родителей нужно выяснить возможный контакт с больным туберкулезом, получить данные о сроках вакцинации и ревакцинации БЦЖ, результаты туберкулиновых проб за предыдущие годы и на обследовании.
Причиной интоксикационного синдрома может быть целый ряд заболеваний, а в непонятных случаях требуется комплексное обследование ребенка. В первую очередь следует исключить интоксикации, связанные с хроническими очагами инфекции полости рта и носоглотки (кариес зубов, синуситы, аденоидиты, хронический тонзиллит).
Состав микобактерии
Микобактерия состоит из клеточной оболочки и цитоплазмы. Клеточная оболочка трехслойная и состоит из наружного, среднего и внутреннего слоев. В вирулентных микобактерий она имеет толщину 230-250 нм.
Внешний слой, окружающий клетку, называют микрокапсулой. Она образована полисахаридами и содержит фибриллы. Микрокапсула может окружать целый популяцию микобактерий, а также помещаться на местах прилегания микобактерий друг к другу. Отсутствие или наличие роста, его интенсивность и состав микрокапсулы зависят от того, какое количество корд-фактора экстрагируется из цитоплазмы в клеточную стенку. Чем больше корд-фактора экстрагируется, тем лучше выражена микрокапсула у микобактерий туберкулеза.
Клеточная оболочка участвует в регуляции метаболических процессов. В ней содержатся видоспецифические антигены, благодаря чему клеточная стенка является локусом, где происходят аллергические реакции повышенной чувствительности замедленного типа и образование антител, поскольку она, как собственно поверхностная структура бактериальной клетки, первой контактирует с тканями макроорганизма.
Под клеточной оболочкой расположена трехслойная цитоплазматическая мембрана, тесно прилегает к цитоплазме. Она состоит из липопротеидных комплексов. В ней происходят процессы, обусловливающие специфичность реакции микобактерий на факторы окружающей среды.
Цитоплазматическая мембрана микобактерий туберкулеза путем своей центростремительной инвагинации формирует в цитоплазме внутрицитоплазматическая мембранную систему — мезос. Мезосомы — полуфункциональные структуры. В них содержится много ферментных систем. Они участвуют в синтезе и формировании клеточной стенки и выполняют роль посредника между ядром и цитоплазмой бактериальной клетки.
Цитоплазма микобактерий состоит из гранул и включений. У молодых микобактерии туберкулеза цитоплазма более гомогенная и компактная, чем у старых, у которых в цитоплазме больше вакуоль и полостей. Основную массу гранулярных включений составляют рибосомы, располагающиеся в цитоплазме в свободном состоянии или образующие полисомы — скопление рибосом. Рибосомы состоят из РНК и белка и синтезируют специфический белок.
Иммуногенность микобактерий туберкулеза обусловлена в основном антигенными комплексами, содержащихся в оболочках микобактериальных клеток. Рибосомы, рибосомный белок и цитоплазма микобактерий имеют антигенную активностью в реакциях замедленного типа.
Лечение
Рис. 4. Схематическое изображение пункции натечника: а — неправильный прокол (слева) с образованием прямого канала (справа), через который при наполнении полости натечника гной может вытекать наружу; б — правильный прокол — сбоку, косо (слева), со смещением кожи, благодаря которому образуется клапанный ход (справа), стрелкой показано направление движения пальца, оттягивающего кожу; e — при плоских натечниках (слева) один край гнойника сдавливают рукой (справа) и пунктируют сбоку.
В период применения исключительно консервативной терапии костно-суставного туберкулеза борьба с Н. осуществлялась с помощью паллиативных средств. Т. П. Краснобаев (1947) и др. считали, что ведущая роль в лечении Н. принадлежит пункциям, к-рые выполняли по определенной методике (рис. 4) с последующим промыванием полости различными антисептическими средствами. Эта леч. тактика оказалась мало состоятельной даже в последующем, когда открылись широкие возможности применения специфических противотуберкулезных препаратов. Расчет на ликвидацию Н. без удаления основного очага в кости не оправдался, как и расчет на его спонтанное излечение. Кардинальное решение проблемы лечения Н. стало возможным только с развитием радикальной хирургии костно-суставного туберкулеза.
Большинство современных авторов рекомендует применять при Н. оперативное лечение с ликвидацией туберкулезного очага в кости — абсцессэктомию и абсцессотомию, к-рые проводят на фоне антибактериальной и общеукрепляющей терапии. Полное удаление Н. вместе с капсулой (абсцессэктомия) выполнимо не при всех его локализациях. Операция, как правило, не представляет трудностей на конечностях, но при спондилите, в частности поясничном, вследствие обширности вмешательства нельзя исключить опасности повреждения соседних органов. При нек-рых же локализациях Н. эта операция технически просто неосуществима. Абсцессотомия (удаление содержимого Н. и его пиогенной оболочки) — более щадящее вмешательство, она обеспечивает не худшие результаты и является менее опасной. В 1953 г. П. Г. Корнев впервые применил абсцессотомию по типу предложенной им ранее (1948) укорачивающей фистулотомии с одновременным кюрета-жем туберкулезных очагов в телах позвонков. Оперативные вмешательства такого рода оказались более эффективными, чем пункции Н.