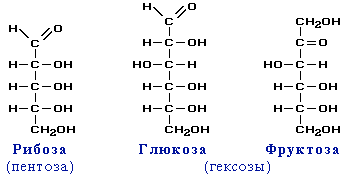Аппаратные методы коррекции фигуры: как гибнут жировые клетки
Содержание:
Разработка
Преадипоциты — это недифференцированные фибробласты, которые можно стимулировать с образованием адипоцитов. Исследования пролили свет на потенциальные молекулярные механизмы в определении судьбы преадипоцитов, хотя точное происхождение адипоцитов все еще неясно. На изменение распределения жира в организме в результате нормального роста влияет нутритивный и гормональный статус, зависящий от внутренних различий в клетках, обнаруженных в каждом жировом депо.
Мезенхимальные стволовые клетки могут дифференцироваться в адипоциты, соединительную ткань , мышцы или кости .
Предшественник взрослой клетки называется липобластом , а опухоль этого типа клеток известна как липобластома .
Абстракт
Наиболее популярными на сегодняшний день аппаратными методами коррекции контуров тела являются: разрушение жировых клеток под действием ультразвука; лазера; холода (криолиполиз) и переменного электрического тока радиочастотного диапазона (RF-воздействие). Эти процедуры отличаются не только разными типами физиотерапевтического воздействия, но разными вариантами гибели адипоцитов. Согласно последней классификации, принято различать типы клеточной смерти не только на основании морфологических изменений, но и согласно биохимическим процессам, протекающим при них. В обзоре рассмотрены основные механизмы реализации эффектов аппаратных методов коррекции контуров тела, а также приведены новейшие данные о биологических аспектах действия «усиленного» RF-липолиза — технологии BodyFX.
Гормональные нарушения заставляют вас толстеть
Если эта система работает так хорошо, то почему же в последнее время появилось так много людей с избыточным весом? Ученые обнаружили, что старение, болезни и нездоровый образ жизни нарушают нормальную работу жироконтролирующих систем. Это сказывается на веществах, регулирующих жировые клетки. Таким образом, вместо того, чтобы помогать нам контролировать вес, гормоны способствуют его увеличению.
В конце 80-х годов, было обнаружено, что нарушения обмена инсулина значительно повышают риск возникновения ожирения и сердечных заболеваний. Инсулин, как и все гормоны, работает, связываясь со специальными рецепторами в клетках. Комбинация неправильного питания, малоподвижного образа жизни и генетического наследия может вызвать проблемы с этими рецепторами. Для того, чтобы компенсировать «медленную работу» рецепторов, поджелудочная железа высвобождает больше инсулина.
Это вызывает множество заболеваний — избыточный вес, высокое кровяное давление, подъем уровня жиров в крови и диабет. Ученые называют этот процесс «метаболический синдром» или Синдром X. {banner_st-d-2}
Отложение жира в абдоминальной области — наиболее опасное проявление синдрома. Абдоминальный жир высвобождает жирные кислоты прямо в печеночный кровоток. Это вызывает повышенную выработку «плохого» холестерина и снижение способности печени к очищению инсулина, что влечет за собой повышение его уровня выше нормы. Так начинается порочный круг: высокий уровень инсулина ведет к ожирению, что вызывает еще большую выработку инсулина. Недавние исследования показали, что лептин (основной регулятор жира) также недостаточно хорошо работает у людей с таким нарушением, как инсулиновая резистентность.
Роль ожирения и отложения жира в абдоминальной области на возникновение метаболического синдрома неясна и противоречива. Некоторые полагают, что проблема заключается в низкой физической активности и содержании большого количества жиров и рафинированных сахаров в диете. Например, такой рацион у животных вызывал появление инсулиновой резистентности уже через несколько недель. Добавление физической нагрузки и изменения в диете вызывали улучшение большинства факторов, связанных с метаболическим синдромом (кровяное давление, инсулин, триглицериды), даже если не наблюдалось снижения веса тела.
Инсулиновая резистентность и высокий уровень инсулина являются скорее причиной, чем следствием ожирения. Уровень липопротеина липазы (энзим, способствующий отложению жира) снижается в скелетных мышцах, кода имеет место инсулиновая резистентность. С другой стороны, в жировых клетках высокие уровни инсулина стимулируют липопротеин липазу, подавляя гормоно-чувствительную липазу (энзим, расщепляющий жиры). Такие изменения могут вызвать снижение метаболизма жиров в мышцах и накопление их в жировых клетках.
Что происходит на микроуровне?
Пластический хирург Диана Дункан (Diane I. Duncan) исследовала механизм клеточной гибели под действием высоковольтных сверхкоротких RF-импульсов. В исследовании приняло участие 12 пациентов, которые прошли 8 процедур липолиза на аппарате BodyFX с интервалом между процедурами 1 неделю. Сканирующая электронная микроскопия адипоцитов в области воздействия выявила, что гибель клеток происходила не по механизмам апоптоза или некроза, а по механизму пироптоза (рис. 4), имеющего характеристики обоих этих процессов и отличающегося наличием воспалительного компонента [].
| A. Нормальный интактный адипоцит | |
| B. Адипоцит спустя 2 недели после 2 процедур BodyFX\TiteFX: в клеточной стенке заметны мелкие трещины | |
| C. Адипоцит через 4 недели после 4 процедур BodyFX\TiteFX: в клеточной стенке множество практически равномерно расположенных пор; небольшие пузырьки под мембраной — это жировые капли, которые выйдут через трещины в клеточной стенке | |
| D. Жировые клетки спустя 8 недель после 8-й (последней) процедуры: не все клетки подверглись воздействию, нормальные адипоциты (слева и сверху справа) прилежат к клеткам, которые потеряли значительное количество цитозоля | |
| E. Показаны жировые капли, которые выталкиваются через поры поврежденной жировой клетки, — эта реакция (порация), наблюдаемая на 8-й неделе, является одним из характерных признаков пироптоза. При апоптозе клеточная мембрана не повреждается. При некрозе происходит ранний лизис клеточной стенки со стремительным высвобождением цитозоля и сильной воспалительной реакцией |
Рис. 4 (a–e). Гибель адипоцитов при коррекции фигуры на аппарате BodyFX []
Термин «пироптоз» впервые ввел в 2001 г. американский ученый из Вашингтонского университета Брэд Куксон (Cookson) и его коллега Молли Брэннан (Brennan) для описания особого типа клеточной смерти, запускаемого в макрофагах, инфицированных бактерией Salmonella typhimurium []. Позднее было установлено, что этот тип гибели клеток характерен не только для макрофагов и не только при инфицировании бактериями. Он находится между противоположными процессами — некрозом и апоптозом, обладая характеристиками обоих процессов. В ходе пироптоза происходит активация каспазы-1, которая за счет ограниченного протеолиза способствует активации и выходу пирогенных ИЛ-1β и ИЛ-18 (рис. 5). Это обусловливает наличие воспалительной реакции разной степени выраженности при данном варианте программируемой клеточной смерти. Однако она будет существенно меньше, чем при некрозе, поскольку весь процесс пироптоза растянут во времени []. Морфологически при пироптозе в клеточной мембране образуются поры диаметром 1,1–2,4 нм, что нарушает клеточный ионный градиент. В результате увеличение осмотического давления вызывает приток воды с последующим набуханием клетки и ее разрывом. В то же время внутреннее содержимое постепенно выходит наружу через эти же поры []. Отличительным признаком пироптозной реакции является полная потеря объема клеткой после первичного отека.
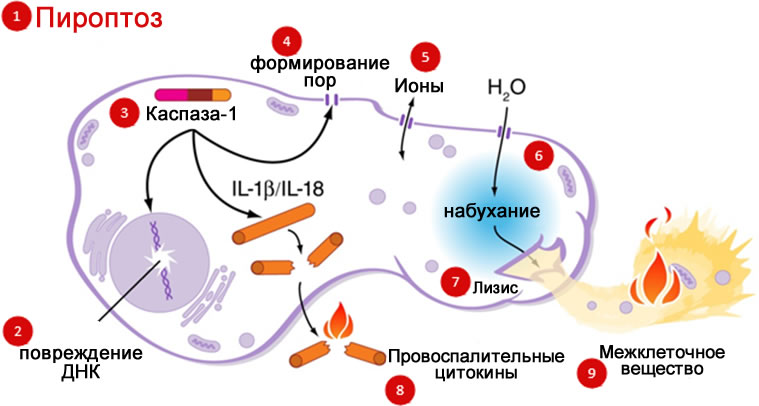
Рис. 5. Схема пироптоза []
При технологии BodyFX\TiteFX RF-воздействие активирует липолитические ферменты и запускает процесс разрушения жиров, а сверхкороткие (наносекундные) высоковольтные импульсы приводят к появлению эффекта необратимой электропорации в мембране жировой клетки. Необратимая электропорация характеризуется образованием многочисленных мельчайших пор в поврежденной клеточной стенке, что очень похоже на ответную реакцию, наблюдаемую при пироптозе. Внеклеточный кальций проникает в эти дефекты, тем самым нивелируя эффективность системы ионной откачки. Затем происходит лизосомальный экзоцитоз. Предварительный нагрев ткани с помощью переменного тока радиочастотного диапазона, вероятно, снижает порог электропорации и делает адипоциты более восприимчивыми [].
Уменьшение проявлений целлюлита с помощью BodyFX \ TiteFX реализуется путем уплотнения кожи в обрабатываемой области за счет неабляционного воспалительного повреждения дермы, ее последующей реструктуризации и синтеза нового коллагена I типа и эластина.
Патологическая анатомия
Патологические изменения в Подкожной жировой клетчатке могут быть связаны с нарушениями жирового обмена. При эндогенных и экзогенных формах ожирения (см.) в П. ж. к. увеличивается количество жировых долек за счет гиперплазии липоцитов и увеличения жира в их цитоплазме (гипертрофия липоцитов). При этом происходит образование новых капилляров, а в самих жировых клетках нередко обнаруживаются деструктивные изменения. Снижение количества жира в цитоплазме жировых клеток отмечается при истощении. При этом ядра клеток занимают центральное положение, их объем часто возрастает.
Мукоидное и фибриноидное набухание соединительной ткани Подкожной Жировой Клетчатки (см. Слизистая дистрофия, Фибриноидное превращение) происходит при коллагеновых болезнях (см.). Амилоидоз (см.) встречается редко. Амилоид может обнаруживаться в стенке сосудов, реже вокруг фолликулов волос, сальных и потовых желез. Кальциноз (см.) возможен на небольших участках, в зоне дистрофических изменений ткани. Напр., при склеродермии (см.) соли кальция откладываются в виде зерен, глыбок или слоистых образований с перифокальной воспалительной реакцией.
Некроз Подкожной Жировой Клетчатки развивается при местных нарушениях кровообращения, механических повреждениях, инъекции некоторых лекарственных средств (напр., р-ров сульфата магния, хлорида кальция и др.) и химических в-в (напр., бензина), при ожогах, отморожениях и т. д. (см. Жировые некрозы, Некроз). В жировых дольках происходит ферментативное расщепление нейтрального жира с образованием жирных кислот и мыл, которые раздражают окружающие ткани, вызывая пери-фокальную продуктивную воспалительную реакцию с наличием гигантских многоядерных клеток (см. Липогранулема).
Артериальная гиперемия Подкожной Жировой Клетчатки чаще возникает при воспалительных процессах в коже и П. ж. к. и носит в основном местный характер. При общем венозном застое в П. ж. к. развивается картина отека. В результате нарушения лимфооттока в П. ж. к. возникают склеротические изменения. Кровоизлияния в П. ж. к. носят разлитой характер и сопровождаются быстрым всасыванием продуктов распада крови.
Неспецифические воспалительные процессы чаще всего носят экссудативный характер — серозный, гнойный, фибринозный. Особое место занимает синдром Пфейффера — Вебера — Крисчена (рецидивирующий ненагнаивающийся спонтанный панникулит), который характеризуется очаговой деструкцией жировой ткани с развитием воспалительной реакции (см. Панникулит). Морфологическая картина специфических воспалительных заболеваний П. ж. к. не отличается от таковой в других органах и тканях (см. Сифилис, Туберкулез внелегочный).
Патологические процессы, вызываемые в П. ж. к. грибками, довольно разнообразны, что зависит от свойств грибков и реакции на них организма. При гистологическом исследовании в П. ж. к. обнаруживаются изменения, свойственные хроническим воспалительным процессам, с особенностями, обусловленными видом возбудителя (см. Микозы).
Атрофия Подкожной Жировой Клетчатки возникает при различных формах кахексии (см.). П. ж. к. приобретает охряно-желтую окраску, что связано с концентрацией пигмента липохрома, жировая ткань пропитывается отечной жидкостью. Гипертрофия П. ж. к. чаще всего бывает викарной, напр, при атрофии мышц конечностей.
Анатомия и гистология
Основу Подкожной жировой клетчатки составляют соединительнотканные фиброзные тяжи, образованные пучками коллагеновых волокон с примесью эластических волокон (см. Соединительная ткань), берущие начало в сетчатом слое кожи (см.) и идущие к поверхностной фасции, к-рая отграничивает П. ж. к. от подлежащих тканей (собственной фасции, надкостницы, сухожилий). По толщине различают фиброзные тяжи 1, 2 и 3-го порядка. Между тяжами 1-го порядка находятся более тонкие тяжи 2-го и 3-го порядка. Ячейки, ограниченные фиброзными тяжами различного порядка, целиком заполнены дольками жировой ткани (см.), образующей жировые отложения (panniculus adiposus). Структура П. ж. к. определяет ее механические свойства — упругость и прочность на растяжение. В местах, подверженных давлению (ладонь, подошва, нижняя треть ягодиц), преобладают толстые фиброзные тяжи, пронизывающие подкожную клетчатку перпендикулярно поверхности тела и образующие удерживатели кожи (retinacula cutis), которые плотно фиксируют кожу к подлежащим тканям, ограничивая ее подвижность. Аналогичным образом кожа волосистой части головы соединяется с сухожильным шлемом. Там, где кожа подвижна, фиброзные тяжи располагаются косо или параллельно поверхности тела, образуя пластинчатые структуры.
Жировые отложения в подкожной клетчатке плода до 7 мес. незначительны, но быстро нарастают к концу внутриутробного периода. В организме взрослого человека они составляют в среднем ок. 80% всей массы П. ж. к. (процент сильно варьирует в зависимости от возраста т пола и особенностей телосложения). Жировая ткань отсутствует лишь под кожей век, полового члена, мошонки, клитора и малых половых: губ. Незначительно ее содержание в подкожной основе лба, носа, наружного уха, губ. На сгибательных поверхностях конечностей содержание жировой ткани больше, чем на разгибательных. Самые большие жировые отложения образуются на животе, ягодицах, у женщин также на груди. Имеется тесная корреляция между толщиной П. ж. к. в различных сегментах конечностей и на туловище. Соотношение толщины П. ж. к. у мужчины и женщины составляет в среднем 1 : 1,89; общая ее масса у взрослого мужчины достигает 7,5 кг, у женщины 13 кг (соответственно 14 и 24% массы тела). В старческом возрасте общая масса жировой ткани под кожей уменьшается и распределение ее становится непропорциональным.
В нек-рых частях тела в П. ж. к. располагаются мышцы, при сокращении к-рых кожа в этих местах собирается в складки. Поперечнополосатые мышцы находятся в подкожной клетчатке лица и шеи (подкожная мышца шеи), гладкие мышцы — в подкожной основе наружных половых органов (особенно в мясистой оболочке мошонки), заднего прохода, соска и околососкового кружка молочной железы.
Подкожная жировая клетчатка богата кровеносными сосудами. Артерии, проникая в нее из подлежащих тканей, образуют густую сеть на границе с дермой. Отсюда их ветви идут в фиброзных тяжах и делятся на капилляры, окружающие каждую жировую дольку. В П. ж. к. образуются венозные сплетения, в к-рых формируются крупные подкожные вены. Лимф, сосуды П. ж. к. берут начало в глубокой лимфатической сети кожи и идут к регионарным лимф, узлам. Нервы образуют широкопетлистое сплетение в глубоком слое П. ж. к. Чувствительные нервные окончания представлены в подкожной ткани пластинчатыми тельцами — тельцами Фатера — Пачини (см. Нервные окончания).
Развитие
Как и другие клетки соединительной ткани, адипоциты происходят от мезенхимальных стволовых клеток. Мезенхимальные стволовые клетки дают начало преадипоцитам, которые похожи на крупные фибробласты с цитоплазматическими липидными включениями. Первоначально липидные капли молодого белого адипоцита изолированы друг от друга, но вскоре они сливаются с образованием единой большой жировой капли. Белые адипоциты развиваются вместе с меньшей популяцией бежевых адипоцитов, которые присутствуют в зрелой белой жировой ткани. При адаптации к низким температурам белые адипоциты частично обратимо превращаются в бурые, приобретают большое количество мелких липидных капель вместо одной крупной, их профиль экспрессии генов становится близок к таковому у бурых адипоцитов (в частности, возрастает экспрессия гена UCP1, кодирующего термогенин), и так называемые бежевые адипоциты приступают к термогенезу. При возвращении к нормальным условиям часть бежевых адипоцитов вновь становятся белыми. У мышей «побурение» белой жировой ткани полностью нивелируется за 21 день после окончания пребывания на холоде, а снижение экспрессии UCP1, кодирующего термогенин, наступает уже через 24 часа. При повторном попадании на холод в бежевые адипоциты превращаются каждый раз одни и те же белые адипоциты. Превращение белого адипоцита в бежевый контролируется несколькими транскрипционными факторами: PPARγ, PRDM16, PGC-1α и EBF2. «Побурение» белого жира также стимулируют иризин, секретируемый мышечной тканью в ответ на физическую нагрузку, и FGF21, выделяемый печенью. У мышей «побурение» стимулируют метионин-энкефалиновые пептиды, продуцируемые лимфоидными клетками врождённого иммунитета 2 типа в ответ на действие интерлейкина 33 (IL-33).
Бурые адипоциты также развиваются от мезенхимальных стволовых клеток, но в других локациях тела эмбриона, отличных от тех, где происходит дифференцировка белых адипоцитов. Бурые адипоциты в ходе эмбрионального развития возникают раньше белых. У человека объём бурой жировой ткани относительно массы тела максимален при рождении, когда наиболее высока потребность в термогенезе, и в детстве почти полностью исчезает через инволюцию и апоптоз адипоцитов. У взрослых бурый жир наиболее активен у людей худощавого телосложения. При адаптации к холоду бежевые адипоциты могут превращаться в бурые, кроме того, возможна пролиферация и дифференцировка бурых адипоцитов от мезенхимальных клеток-предшественников. Автономные нервы не только стимулируют термогенную активность бурых адипоцитов, но также способствуют их дифференцировке и предотвращают апоптоз зрелых бурых адипоцитов.
Строение
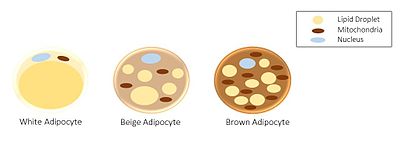
Морфология адипоцитов трёх видов: белого, бежевого и бурого
Клетки жировой ткани, накапливающие жир, называют адипоцитами. Одиночные адипоциты имеют шарообразную форму. Жировую ткань принято подразделять на белую и бурую согласно её цвету. Адипоцит белой жировой ткани содержит одну большую каплю нейтрального жира (такие адипоциты также называют унилокулярными), которая занимает центральную часть клетки и окружена тонким слоем цитоплазмы, в утолщённой части которого залегает уплощённое ядро. В цитоплазме адипоцитов содержатся в небольших количествах и другие липиды: холестерин, фосфолипиды, а также свободные жирные кислоты. Эти мелкие жировые включения особенно выражены у незрелых адипоцитов. Зрелый адипоцит имеет крупные размеры, от 50 до 150 мкм. Так как липиды вымываются ксиленом и другими растворителями, использующимися при приготовлении гистологических препаратов, унилокулярные адипоциты при рассмотрении с помощью светового микроскопа выглядят пустыми.
Рыхлая волокнистая соединительная ткань образует прослойки, которые делят жировую ткань на дольки разного размера и формы. В дольках адипоциты близко прилегают друг к другу, однако в жировой ткани также присутствуют клетки так называемой стромальной васкулярной фракции: преадипоциты, фибробласты, клетки эндотелия сосудов и ряд иммунных клеток, такие как макрофаги жировой ткани. На клетки стромальной васкулярной фракции приходится около половины всех клеток жировой ткани. Жировые клетки разделяются тонкими коллагеновыми волокнами, ориентированными во всех направлениях, а также оплетены ретикулярными волокнами. Группы адипоцитов или отдельные дольки тесно охватываются кровеносными и лимфатическими капиллярами.
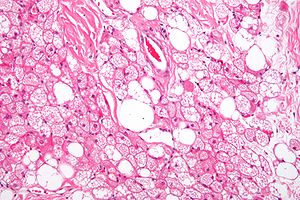
Микрофотография гиберномы — доброкачественной опухоли, состоящей из бурых адипоцитов
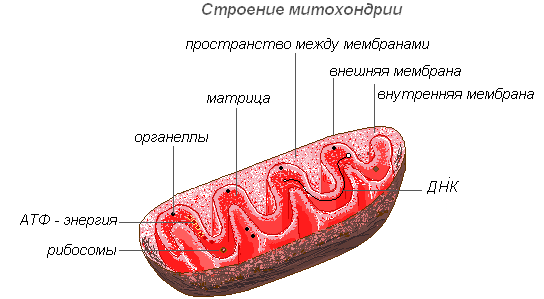
У новорождённых детей и некоторых животных (грызунов и животных, впадающих в спячку) выражена бурая жировая ткань. Адипоциты бурой жировой ткани, по сравнению с клетками белой жировой ткани, имеют больше митохондрий и вместо одной крупной жировой капли содержат множество мелких жировых включений в цитоплазме (такие адипоциты называют мультилокулярными). Бурый цвет обеспечивается железосодержащими пигментами цитохромами, расположенными в митохондриях. Изменения бурой жировой ткани при голодании выражены меньше, чем белой.
Термином «бежевый жир» называют белую жировую ткань, которая приобретает некоторые черты бурой жировой ткани, например, в её адипоцитах вместо одной крупной жировой ткани имеется несколько включений меньшего размера, увеличивается количество митохондрий и повышается уровень экспрессии гена UCP1, кодирующего белок термогенин.
Четвёртый тип адипоцитов был недавно описан в составе подкожной жировой ткани мышей во время беременности и лактации, когда жировая ткань в молочных железах существенно сокращается, а железистая часть, наоборот, разрастается. Новосформированные эпителиальные клетки, входящие в состав железистой части, называют розовыми адипоцитами. Они появляются в результате прямой трансдифференцировки белых адипоцитов в эпителиальные клетки, продуцирующие молоко. Образование розовых адипоцитов обратимо, и по завершении лактации они превращаются обратно в белые адипоциты, восстанавливая жировую часть молочной железы.
Плотность жировой ткани составляет около 0,9 г/мл против 1,06 г/мл для мышечной ткани, поэтому человек, имеющий больше жира, будет держаться на воде легче, чем человек того же веса, но с большей мышечной массой.
Жировые клетки. Как устроены клетки жировой ткани?
30.05.2021, просмотров: 2020
Жировая клетка называется «адипоцит». Это название состоит из латинского элемента «adeps», что означает «жир», и греческого элемента «kytos», что значит «полый пузырек». Клетки жировой ткани при их изучении под сканирующим электронным микроскопом имеют вид шариков, окруженных коллагеновыми волокнами и кровеносными капиллярами.
Клетки белой и бурой жировой ткани значительно отличаются друг от друга. Клетка белой жировой ткани имеет внутри себя один большой жировой пузырек. Этот жировой пузырек занимает практически всю клетку, оттесняя на периферию ядро клетки, которое становиться сплюснутым.
В процессе эмбрионального развития жировая ткань развиваются из так называемой мезенхимы, то есть эмбриональной соединительной ткани. Мезенхима дает начало всем остальным видам соединительной ткани, в том числе и жировой ткани. Мезенхимальная клетка превращается в липобласт, который в свою очередь, превращается в зрелую жировую клетку — адипоцит.
Интересно, что человек относится к немногим млекопитающим, которые рождаются уже с жировыми отложениями. Они начинают появляться на 30 неделе внутриутробного развития. Раньше считалось, что человек рождается уже с готовыми жировыми клетками, и число их у взрослых людей н увеличивается. В настоящее время выяснено, что это н так. Действительно, сами зрелые жировые клетки н делятся, однако на протяжении всей жизни у человека сохраняются клетки-предшественники жировых клеток.
Существует два периода активного размножения жировых клетокпредшественников, и соответственно, увеличения количества адипоцитов:
- период эмбрионального развития
- период полового созревания.
В другие периоды жизни человека обычно размножения клеток-предшественниковн происходит. Накопление жира происходит только путем увеличения размеров уже существующих жировых клеток. Такой рост жировой ткани называется гипертрофическим.
Однако, никакая клетка н может увеличиваться до бесконечности. Когда количество жира в клетке достигает критической массы, клетки-предшественники получают сигнал, и начинают размножаться, давая рост новым жировым клеткам. Такой тип роста жировой ткани, за счет увеличения количества жировых клеток, называется гиперпластическим (гиперцеллюлярным). Он может иметь место в любом возрасте. Так, у худого взрослого человека имеется около 35 миллиардов жировых клеток. У человека, имеющего выраженное ожирение, количество жировых клеток может достигать 125 миллиардов, то есть в 4 раза больше. Вновь образованные жировые клетки обратному развитию н подлежат, и сохраняются на всю жизнь. Если человек худеет, то они лишь уменьшаются в размерах.
Тиреоидный гормон, гормон роста, кортизол и тестостерон
Эти гормоны также играют немалую роль в синтезе жиров. Взрослые люди часто теряют вес после инъекций тиреоидного гормона, гормона роста или тестостерона, особенно в случаях, когда их естественный уровень до этого был низок. Тиреоидные гормоны повышают темп химических реакций почти во всех клетках нашего организма, но главный эффект оказывают на метаболизм. Гормон роста и кортизол ускоряют высвобождение жиров из жировых клеток. Они также заставляют организм больше использовать жир в качестве топлива. Тестостерон, главный мужской гормон, также снижает содержание жира в теле человека.
Опасный ген ожирения
Ученые из Каролинского института в Швеции в ходе недавнего исследования сумели выявить ген, который отвечает за развитие наиболее опасного жира в человеческом организме (в плане осложнений). По словам научных специалистов, данный ген может являться фактором риска развития сахарного диабета 2 типа и инсулинорезистентности.
Бурая и белая жировая ткань
Белая жировая ткань, считающаяся «плохим» жиром организма, подразумевает рыхлую ткань, состоящую в большинстве своем из адипоцитов. Данные жировые клетки отвечают за выполнение функции сохранения и в дальнейшем высвобождения энергии в человеческом организме.
ВАЖНО: В женском организме жировая ткань составляет около четверти всей массы тела, подкожно-жировой слой имеет большую толщину, чем у мужчин, а жиры откладываются в области бедер, груди и таза. У человека имеется две разновидности жировой ткани: бурый и белый жир
В последнее время бурая жировая ткань считается «хорошим» жиром организма. По словам специалистов науки, основная роль бурого жира состоит в накоплении и выработке энергии с целью обеспечения физиологических процессов. Ученым удалось выяснить, что люди с весом в норме склонны к накоплению бурой жировой ткани, служащей субстратом энергии при физических нагрузках
У человека имеется две разновидности жировой ткани: бурый и белый жир. В последнее время бурая жировая ткань считается «хорошим» жиром организма. По словам специалистов науки, основная роль бурого жира состоит в накоплении и выработке энергии с целью обеспечения физиологических процессов. Ученым удалось выяснить, что люди с весом в норме склонны к накоплению бурой жировой ткани, служащей субстратом энергии при физических нагрузках.
Белая жировая ткань может накапливаться в подкожной клетчатке в избыточном количестве у людей, имеющих избыточный вес или страдающих от ожирения.
Ученые из Швеции утверждают, что увеличенное число и размер адипоцитов может вызвать чрезмерное накопление белой жировой ткани и повышает риск развития сахарного диабета 2 типа. В недавнем исследовании ученые установили, что гипертрофия адипоцитов может быть связана с геном EBF1, низкий уровень экспрессии которого провоцирует инсулинорезистентность.
Ген, вызывающий ожирение
В ходе исследовательской деятельности ученые проводили анализ жировой ткани участников с крупными и мелкими жировыми клетками. Было выявлено, что у пациентов с крупными жировыми клетками экспрессия гена EBF1 в жировой ткани снижена по сравнению с пациентами, адипоциты которых имели малый размер. Кроме этого, у лиц с крупными адипоцитами отмечается изменение липидного транспорта и инсулинорезистентность, что говорит о высоком риске развития сахарного диабета по причине повышения в крови уровня глюкозы и липидов.
В дальнейшем ученые проводили эксперименты на мышах со специально сниженной экспрессией гена EBF1. Результатом стала гипертрофия адипоцитов и высвобождение липидов. После питания мышей продуктами с высоким жировым содержанием появлялась инсулинорезистентность.
Новые возможности науки
По мнению ученых, ген EBF1 связывается с белком, управляющим другими генами, регулирует образование адипоцитов и контролирует метаболизм. По словам профессора Петра Арнера, данные результаты могут создать новые возможности для лечения сахарного диабета 2 типа.
По словам профессора, в скором времени будут разработаны новые препараты, улучшающие обмен веществ и функцию гена EBF1 в жировой ткани организма человека. Благодаря этому в будущем могут быть найдены новые пути лечения сахарного диабета 2 типа.
https://youtube.com/watch?v=2HPbW1uigz0
Эта проблема объединяет множество женщин в мире и, хоть она и неопасна для здоровья, но сводит на «нет» все достижения и успехи женской красоты. Благодаря этому …
Читать далее >>
История
В 1876 году Карл Фон Купфер описал клетки, названные им «Sternzellen» (звёздчатые клетки). При окрашивании оксидом золота, в цитоплазме клеток были заметны включения. Ошибочно сочтя их фрагментами эритроцитов, захваченных путём фагоцитоза, Купфер в 1898 году пересмотрел свои взгляды о «звёздчатой клетке» как об отдельном типе клеток и отнес их в разряд фагоцитов. Однако в последующие годы регулярно появлялись описания клеток, похожих на Купферовские «звёздчатые клетки». Им присваивались различные названия: интерстициальные клетки, парасинусоидные клетки, липоциты, перициты. Роль этих клеток оставалась загадкой на протяжении 75 лет, пока профессор Тосио Ито (Toshio Ito) не обнаружил в перисинусоидальном пространстве печени человека некие клетки, содержащие вкрапления жира. Ито назвал их «shibo-sesshu saibo» — жиропоглощающие клетки. Поняв, что вкрапления были жиром, выработанным клетками из гликогена, он сменил название на «shibo-chozo saibo» — жирозапасающие клетки.В Кендзиро Вакэ (Kenjiro Wake) доказал идентичность «Sternzellen» Купфера и жирозапасающих клеток Ито. Вакэ также установил, что эти клетки выполняют важную роль складирования витамина А (до этого считалось, что витамин А откладывается в клетках Купфера). Вскоре после этого, Кент и Поппер продемонстрировали тесную связь клеток Ито с фиброзом печени. Эти открытия положили начало процессу детального изучения клеток Ито.

Вверху — схематическое изображение клетки Ито (HSC) по соседству с ближайшими гепатоцитами (PC), ниже синусоидальных эпителиальных клеток печени (EC). S — синусоид печени; KC — клетка Купфера. Внизу слева — клетки Ито в культуре под световым микроскопом. Внизу справа — электронная микроскопия позволяет разглядеть многочисленные жировые вакуоли (L) клеток Ито (HSC), в которых хранятся ретиноиды.
- Wake, K. (1988) Liver perivascular cells revealed by gold- and silver-impregnation method and electron microscopy. In «Biopathology of the Liver. An Ultrastructural Approach» (Motta, P. M., ed) pp. 23-36, Kluwer Academic Publishers, Dordrecht, Netherlands
- Querner F: Der mikroskopische Nachweis von Vitamin A im animalen Gewebe. Zur Kenntnis der paraplasmatischen Leberzellen-einschlüsse. Dritte Mitteilung. Klin Wschr 1935, 14:1213-1217.
Функции бурой и белой жировой ткани в организме
Каждая из вышеуказанных тканей имеет различные функции в организме – белая жировая ткань хранит энергию, тогда как бурая ткань отвечает за термогенез.
Белая жировая ткань образует изоляционные слои. Энергия накапливается в виде триглицеридов (ТГ), которые защищают организм от потери энергии в виде тепла. С другой стороны, бурая жировая ткань отвечает за метаболические процессы, в том числе производство тепла, которое затем распределяется по всему телу для поддержания постоянной температуры.{banner_st-d-1}
Основное функциональное различие между тканями заключается в том, что белый хранит энергию в виде ТГ, а бурый – липиды для получения энергии.
Тепло в бурой жировой ткани производится главным образом в процессе сжигания длинноцепочечных жирных кислот. Выделенные протоны переносятся через UCP-1 (специфический разобщающий белок) в митохондрии (исключая окислительное фосфорилирование и путь синтеза АТФ), что, в свою очередь, приводит к высвобождению энергии в виде тепла.