Костная ткань
Содержание:
Разработка
Летопись окаменелостей показывает, что остеоциты присутствовали в костях бесчелюстных рыб 400–250 миллионов лет назад. Было показано, что размер остеоцитов зависит от размера генома; и это соотношение использовалось в палеогеномных исследованиях.
Во время формирования кости остеобласт остается позади и погружается в костный матрикс в качестве «остеоид-остеоцита», который поддерживает контакт с другими остеобластами посредством расширенных клеточных процессов. Процесс остеоцитогенеза в значительной степени неизвестен, но было показано, что следующие молекулы играют решающую роль в производстве здоровых остеоцитов, либо в правильном количестве, либо в определенном распределении: матриксные металлопротеиназы (MMP), белок матрикса дентина 1 (DMP-1) , фактор остеобластов / остеоцитов 45 (OF45), Klotho , TGF-бета-индуцибельный фактор (TIEG), лизофосфатидная кислота (LPA), антиген E11 и кислород. 10–20% остеобластов дифференцируются в остеоциты. Те остеобласты на поверхности кости, которые предназначены для захоронения, поскольку остеоциты замедляют выработку матрикса и захоронены соседними остеобластами, которые продолжают активно продуцировать матрикс.
Электронное изображение HAADF-STEM созревающего остеоцита (преостеоцита или остеоид-остеоцита) на поверхности кости, появляющегося непосредственно над остеобластоподобными клетками-предшественниками (декальцинированный матрикс)
Обратите внимание на удлиненные клеточные отростки, которые окружены матрицей коллагена типа I (секретируемой остеобластами), уже пересекающей ламеллярные границы, поскольку коллаген (и, в конечном итоге, минерал) продолжает поглощать клетку. На этой стадии дифференцировки клетка будет экспрессировать такие молекулы, как E11 / gp38, MEPE, PHEX и, возможно, в некоторой степени DMP1, но не склеростин
Palumbo et al. (1990) различают три типа клеток от остеобласта до зрелого остеоцита: преостеоцит типа I (остеобластический остеоцит), преостеоцит типа II (остеоид-остеоцит) и преостеоцит типа III (частично окруженный минеральным матриксом). Встроенный «остеоид-остеоцит» должен выполнять две функции одновременно: регулировать минерализацию и формировать соединительные дендритные отростки, что требует расщепления коллагена и других молекул матрикса. Превращение подвижного остеобласта в захваченный остеоцит занимает около трех дней, и за это время клетка производит объем внеклеточного матрикса, в три раза превышающий собственный клеточный объем, что приводит к уменьшению объема тела зрелой клетки остеоцита на 70% по сравнению с исходным. объем остеобласта. Клетка претерпевает резкое превращение из многоугольной формы в клетку, которая расширяет дендриты к фронту минерализации, за которыми следуют дендриты, которые простираются либо до сосудистого пространства, либо до поверхности кости. Когда остеобласт превращается в остеоцит, щелочная фосфатаза снижается, а казеинкиназа II повышается, как и остеокальцин .
Остеоциты, по-видимому, обогащены белками, устойчивыми к гипоксии, что, по-видимому, связано с их встроенным расположением и ограниченным поступлением кислорода. Напряжение кислорода может регулировать дифференцировку остеобластов в остеоциты, а гипоксия остеоцитов может играть роль в резорбции кости, опосредованной неиспользованием.
Клеточное строение
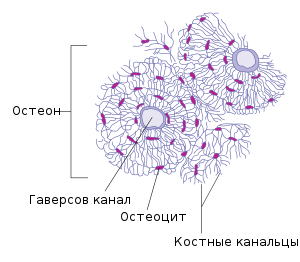
Микроскопическая структура кости
По микроскопическому строению костное вещество представляет особый вид соединительной ткани (в широком смысле слова), костную ткань, характерные признаки которой: твёрдое, пропитанное минеральными солями волокнистое межклеточное вещество и звездчатые, снабжённые многочисленными отростками, клетки.
Основу кости составляют коллагеновые волокна, окруженные кристаллами гидроксиапатита, которые слагаются в пластинки. Пластинки эти в костном веществе частью располагаются концентрическими слоями вокруг длинных разветвляющихся каналов (Гаверсовы каналы), частью лежат между этими системами, частью обхватывают целые группы их или тянутся вдоль поверхности кости. Гаверсов канал в сочетании с окружающими его концентрическими костными пластинками считается структурной единицей компактного вещества кости — остеоном. Параллельно поверхности этих пластинок в них расположены слои маленьких звездообразных пустот, продолжающихся в многочисленные тонкие канальцы — это так называемые «костные тельца», в которых находятся костные клетки, дающие отростки в канальцы. Канальцы костных телец соединяются между собой и с полостью Гаверсовых каналов, внутренними полостями и надкостницей, и таким образом вся костная ткань оказывается пронизанной непрерывной системой наполненных клетками и их отростками полостей и канальцев, по которым и проникают необходимые для жизни кости питательные вещества. По Гаверсовым каналам проходят тонкие кровеносные сосуды (обычно артерия и вена); стенка Гаверсова канала и наружная поверхность кровеносных сосудов одеты тонким слоем эндотелия, а промежутки между ними служат лимфатическими путями кости. Губчатое костное вещество не имеет Гаверсовых каналов.
Костная ткань рыб представляет некоторые отличия: Гаверсовых каналов здесь нет, а канальцы костных телец сильно развиты.
Остеобласты
Остеобласты — молодые остеобразующие клетки костей (диаметр 15-20 мкм), которые синтезируют межклеточное вещество — матрикс. По мере накопления межклеточного вещества остеобласты замуровываются в нём и становятся остеоцитами. Родоначальником являются адвентициальные клетки.
Остеоциты
Остеоциты — клетки костной ткани позвоночных животных и человека, значительно или полностью утратившие способность синтезировать органический компонент матрикса.
Они имеют отростчатую форму, округлое плотное ядро и слабобазофильную цитоплазму. Органоидов мало, клеточного центра нет — клетки утратили способность к делению. Они располагаются в костных полостях, или лакунах, повторяющих контуры остеоцита, и имеют длину 22-25 мкм, а ширину 6-14 мкм. Во все стороны от лакун отходят слегка ветвящиеся канальцы костных полостей, анастомозирующие (сообщающиеся) между собой и с периваскулярными пространствами сосудов, идущих внутри кости. В пространстве между отростками остеоцитов и стенками канальцев содержится тканевая жидкость, движению которой способствуют «пульсирующие» колебания остеоцитов и их отростков. Остеоциты — единственная живая и активно функционирующая клетка в зрелой костной ткани, их роль заключается в стабилизации органического и минерального состава кости, обмене веществ (в том числе в транспортировке ионов Са из кости в кровь и обратно). Костная ткань, не содержащая живых остеоцитов, быстро разрушается.
Остеокласты
Клетки гематогенного происхождения, образующиеся из моноцитов. Может содержать от 2 до 50 ядер. Организация остеокласта адаптирована к разрушению кости. В сочетании с остеобластами, остеокласты контролируют количество костной ткани (остеобласты создают новую костную ткань, а остеокласты разрушают старую)
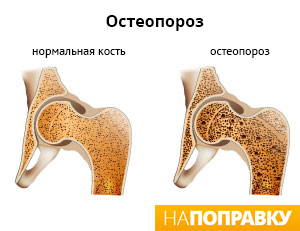
Осложнения от остеопороза
Основное осложнение – это травмы опорно-двигательного аппарата, особенно компрессионные переломы позвоночника и микропереломы из-за резкого сдавления суставов. При этом не обязательна большая нагрузка, можно просто споткнуться и упасть, вследствие чего получить перелом.
На фоне переломов позвоночника может возникать сдавливание спинного мозга и нервных окончаний. Из-за этого возможна утрата чувствительности различных участков тела, а также паралич и инвалидизация.
Особенно опасны переломы в пожилом возрасте – только 9% людей (согласно статистике по РФ) возвращаются к нормальной жизни после этого.
Также остеопороз может иметь следующие последствия:
препятствие росту, что особенно важно для ребенка или подростка;
снижение роста – примерно на 2-4 см в год;
нарушение осанки – «горб» в грудном отделе (грудной кифоз);
нарушение работы внутренних органов из-за неправильной осанки.
Диагностика остеопороза
Проверить состояние организма и подтвердить или исключить диагноз «остеопороз» можно с помощью лабораторных анализов и инструментальных исследований, из которых наиболее проста и информативна – денситометрия.
Лабораторные анализы:
- кальций в моче;
- клинический анализ крови;
- щелочная фосфатаза (показатель биохимии);
- ТТГ;
- маркеры костного разрушения;
- для мужчин – тестостерон.
Инструментальные методы:
- рентгенография;
- денситометрия;
- биопсия костной ткани;
- сцинтиграфия костей;
- МРТ.
Как проверить, есть ли остеопороз, с помощью денситометрии?
Ультразвуковая денситометрия – быстрый и безболезненный способ диагностики. Во время процедуры измеряется скорость распространения УЗ-волн по костной ткани. По более плотным костям ультразвук проходит быстрее. Результат исследования фиксируется компьютером, показатели сравниваются с нормой. Сеанс длится 2-3 минуты, сразу выдается заключение.
Для проведения этой диагностики применяется денситометр Sonost-3000 – оборудование экспертного уровня, которое может выявить потерю даже 2-5% костной массы.
Денситометрия рекомендована:
- нерожавшим женщинам;
- женщинам старше 45-ти лет;
- женщинам, родившим 2-х и более детей;
- в периоде ранней менопаузы;
- при нарушении менструального цикла;
- при наличии вредных привычек;
- мужчинам после 50-ти лет;
- в случае дефицита половых гормонов.
Обязательно нужно пройти УЗ-денситометрию, если:
- часто случаются переломы;
- был длительный курс глюкокортикостероидов, мочегонных средств, противосудорожных препаратов и антикоагулянтов;
- диагностирован гиперпаратиреоз или другие нарушения функции паращитовидных желез.
Также показаниями служат:
- изменение осанки;
- костные и мышечные боли на фоне перемены погоды;
- боли в пояснице и груди при статической нагрузке;
- старческая сутулость;
- ночные судороги в ногах;
- разрушение зубов;
- снижение роста;
- дефицит массы тела;
- остеопороз у близких родственников;
- низкий уровень тестостерона у мужчин;
- и др.
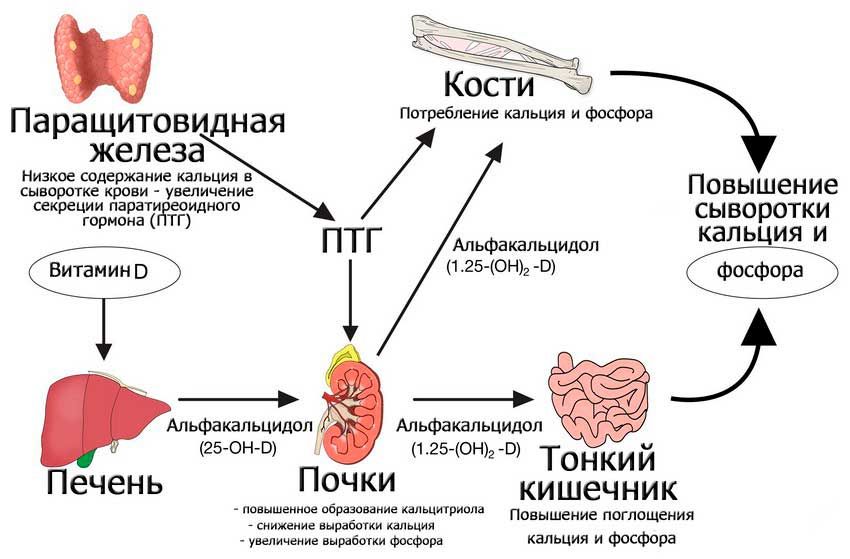
Дефицит кальция в организме человека
Низкий уровень кальция в сыворотке крови — гипокальциемия. Это состояние встречается часто, но в основном протекает бессимптомно. Частая причина гипокальциемии — дефицит витамина Д, необходимого для попадания кальция в кровеносную систему.
Без достаточного количества витамина Д организм не может эффективно усваивать кальций, даже если рацион богат им. Среди других причин дефицита кальция — недостаток кальция в рационе, а также гипопаратиреоз или низкий уровень паратиреоидного гормона.
Хронический низкий уровень кальция может привести к развитию остеопороза, при котором снижается плотность и масса костей. Это увеличивает риск переломов и чаще встречается у людей в возрасте от 60 лет.
Узнайте о ваших рисках развития остеопороза с помощью Генетического теста Атлас.
Симптомы нехватки кальция
Симптомы низкого содержания кальция могут различаться по степени тяжести. Внешний показатель дефицита — состояние ногтей, волос и кожи. Говорить о нехватке также могут неврологические признаки, которые требуют медицинской помощи: онемение, потеря памяти или судороги.
Если у вас наблюдается один или несколько симптомов, перечисленных ниже, это может говорить о том, что организму не хватает кальция:
| Ломкость зубов, ногтей и волос | Головокружение и потеря сознания |
| Нарушение глотания | Боли в области позвоночника и таза |
| Головокружение и потеря сознания | Компрессионный перелом |
| Беспокойство, раздражительность | Уменьшение роста |
| Пониженное артериальное давление | Спазмы легких |
В краткосрочной перспективе последствия не очевидны, но если долго игнорировать симптомы, это может привести к остеопорозу.
Гипокальциемию не следует лечить самостоятельно, так как легко превысить рекомендуемую норму кальция, что может иметь серьезные последствия для организма.
Причины нехватки кальция и развития остеопороза
На уровень кальция в организме влияет не только питание, но и многие другие факторы. Вот некоторые причины, которые повышают риск дефицита кальция и последующего развития остеопороза:
| Фактор | Влияние на уровень кальция |
|---|---|
| Низкий уровень физической активности | Образ жизни с низким уровнем физической активности может вызвать дефицит кальция. |
| Табак и алкоголь | Курение и регулярное употребление алкоголя негативно влияют на плотность костных тканей. |
| Женский пол | Максимальная костная масса у женщин ниже, чем у мужчин, поэтому риски развития остеопороза у женщин выше. |
| Возраст | Люди старше 60 лет больше подвержены риску снижения плотности костных тканей и развитию остеопороза. |
| Происхождение и наследственность | Люди азиатского происхождения, а также люди с семейной историей остеопороза более подвержены риску его развития. |
| Нарушения пищевого поведения | Резкое ограничение пищи при расстройствах пищевого поведения как анорексия и булимия, а также низкий вес, ослабляют кости как у женщин, так и у мужчин. |
| Низкий ИМТ | При показателе индекса массы тела 19 и ниже, риск снижения костной ткани увеличивается. |
| Некоторые лекарственные препараты | Длительный прием некоторых средств как кортикостероиды, препараты для лечения рака груди, противосудорожные средства, снижают прочность костей. |
| Целиакия | При непереносимости глютена всасываемость некоторых нутриентов в кишечнике, включая кальций, замедляется. Если целиакию не лечить, это может привести к остеопорозу. |
Показания и противопоказания к наращиванию кости
Костная пластика назначается в следующих клинических ситуациях:
- Повреждения и травмы челюсти любого типа, которые видны врачу невооруженным глазом, либо на панорамных рентгеновских снимках.
- Подготовка к двухэтапной имплантации – классические методы вживления титановых штифтов не подходят даже при минимальном дефиците ткани.
Как и любая сложная операция, процедура имеет ряд противопоказаний:
- Злокачественные новообразования.
- ВИЧ, туберкулез и другие серьезные заболевания.
- Гайморит и ангина – операцию откладывают до полного выздоровления.
- Индивидуальная непереносимость обезболивающих препаратов.
- Нарушения свертываемости крови.
- Эпилепсия и психические расстройства.
Беременность и кормление грудью давно не являются строгим противопоказанием для проведения костной пластики. Современные методы позволяют решить проблему без последствий, как для матери, так и для будущего ребенка. Единственное ограничение – сроки, вся терапия должна проводиться строго во II триместре.
Беременность не являются противопоказанием для проведения костной пластики
Диагностика остеомаляции
Диагностика заболевания складывается из анализа данных анамнестических,
физикальных, лабораторных и инструментальных методов исследования
При
сборе анамнеза у пациента специалист обращает особое внимание на
длительность течения заболевания, наличие переломов ребер, позвонков,
длинных трубчатых костей, не связанных с существенной травмой. При
осмотре больного пальпаторным путем выявляется болезненность в зоне
проекции отдельных костей, искривление позвоночника, деформации грудной
клетки и таза, мышечная слабость и атрофия мышц.
При анализе лабораторных данных в зависимости от результатов можно
предположить ту или иную форму остеомаляции. Так, например, при снижении
уровня фосфатов в крови ниже нормы, снижении концентрации кальцидиола и
увеличении паратгормона можно предположить, что первопричиной
остеомаляции выступает дефицит витамина Д, который может быть
алиментарным или возникнуть в результате нарушения его всасывания в
пищеварительном тракте. Если количество фосфатов в крови снижено наряду с
увеличенным клиренсом фосфатов, можно предположить первичную потерю
фосфатов или синдром Фанкони.
Если остеомаляция обусловлена проксимальным почечным канальцевым
ацидозом, в крови будет обнаруживаться повышенный уровень соединений
хлора и гипофосфатемия, а впоследствии гиперкальциурия, вызванная
ацидозом. При аксиальной остеомаляции и несовершенном фибриногенезе ни
один из показателей кальция, фосфора и щелочной фосфатазы не выходит за
границы нормы.
Самым информативным из инструментальных методов исследования является
рентгенография. На рентгенограмме взрослых можно увидеть расширение
костномозгового канала и утончение надкостницы длинных трубчатых костей.
В метафизах костей вместо крупных костных ячеек присутствуют участки
мелкоячеистого рисунка. Тела позвонков имеют двояковогнутую форму, а
диски увеличены и имеют двухконтурный рисунок — «рыбьи позвонки».
Одним из наиболее характерных рентгенологических симптомов остеомаляции
являются трещины со склеротически измененными краями шириной до 5 мм,
которые располагаются симметрично и перпендикулярны надкостнице. Это так
называемые псевдопереломы Лоозера. Располагаются они обычно в диафизе
трубчатых костей, в костях таза, лопатках, ключицах, ребрах. При
сканировании они определяются как «горячие» пятна.
При вторичном гиперпаратиреозе характерными рентгенологическими
признаками выступают поднадкостничное рассасывание концевых фаланг и
концевых отделов трубчатых костей, кисты костей.
В силу сходства рентгенологических признаков остеомаляцию следует
дифференцировать от системного остеопороза, для которого более
характерно наличие компрессионных переломов. До момента проявления
признаков на рентгеновском снимке дефект минерализации костей может
выявляться с помощью монофотонной абсорбциометрии, позволяющей
произвести количественную оценку содержания кальция и фосфора в костях
голени и предплечья. Для проведения подобного исследования в позвонках и
шейках бедренных костей проводят двуфотонную абсорбциометрию. При
остеомаляции снижение количества минералов не зависит от возраста или
пола пациентов, а также от формы остеомаляции.
Скорость образования костной ткани и кальцификации можно оценить с
помощью гистоморфометрии с использованием двойной тетрациклиновой метки.
Прогноз и Профилактика
Прогноз благоприятный.
Профилактика начинается еще до рождения ребенка и заключается в строгом соблюдении режима труда, отдыха и питания беременных. Витамин D с целью антенатальной профилактики Р. следует назначать беременным только при наличии у них клин, симптомов D-гиповитаминоза и нарушения фосфорно-кальциевого обмена, а также беременным с экстрагенитальной патологией (заболеваниями печени, почек, жел.-киш. тракта, ревматизмом и поражениями сердечно-сосудистой системы), при патологическом течении беременности (токсикозы первой и второй половины). Витамин D назначают с 28—30-й нед. беременности ежедневно. Суточная доза определяется индивидуальными особенностями беременной, временем года, климатогеографическими условиями.
Профилактику Р
у ребенка начинают с первых дней жизни, уделяя особое внимание неспецифическим профилактическим мероприятиям (правильному уходу, рациональному вскармливанию, максимальному пребыванию на свежем воздухе, проведению закаливающих процедур).. Специфическую профилактику Р
назначают с учетом состояния здоровья ребенка при рождении, особенностей его костной системы, характера вскармливания, условий жизни. Начинать специфическую профилактику следует доношенным детям с 3 — 4-недельного, недоношенным с 2-недельного возраста. Профилактическая доза на курс составляет 150 000 — 300 000 ME витамина D. Рекомендуется ежедневное введение витамина D в дозе 400—500 ME на протяжении всего первого года жизни.
Специфическую профилактику Р. назначают с учетом состояния здоровья ребенка при рождении, особенностей его костной системы, характера вскармливания, условий жизни. Начинать специфическую профилактику следует доношенным детям с 3 — 4-недельного, недоношенным с 2-недельного возраста. Профилактическая доза на курс составляет 150 000 — 300 000 ME витамина D. Рекомендуется ежедневное введение витамина D в дозе 400—500 ME на протяжении всего первого года жизни.
Для искусственного и раннего смешанного вскармливания используют питательные смеси, обогащенные витамином D — «Малютка», «Малыш», «Виталакт» (см. Молочные смеси).
На втором году жизни в осенне-зимний период детям с профилактической целью назначают 1—2 курса УФ-облучения по 20—25 сеансов каждый (см. Ультрафиолетовое излучение) или цитратную смесь с одновременным введением половинной дозы витамина D и витаминов группы В. Во избежание D-витаминной интоксикации не рекомендуется одновременно применять витамин D и УФ-облучение.
Дети, перенесшие Рахит, должны находиться под диспансерным наблюдением не менее 3 лет, при этом в первые 2 года они нуждаются в систематическом проведении комплексного противорецидивного и реабилитационного лечения.
Библиография:
Гинзбург Е. Я. и Сорочек Р. Г. Лечебная гимнастика и массаж при рахите и гипотрофии, М., 1952; Дулицкий С. О. Рахит, М., 1953; Ивановская Т. Е. и Цинзерлинг А. В. Патологическая анатомия (болезни детского возраста), с. 38, М., 1976; Лечебная физкультура при заболеваниях в детском возрасте, под ред. С. М. Иванова, М., 1975; Максудов Г. Б. и др. О рентгенодиагностике костных изменений при витамин-D-зависимом рахите у детей, Вопр. охр. мат. и дет., т. 26, № 10, с. 68, 1981; Панов Н. А., Гингольд А. 3. и Москачева К. А. Рентгенодиагностика в педиатрии, с. 151 и др., М., 1972; Святкина К. А. Актуальные вопросы борьбы с рахитом, Педиатрия, в. 9, с. 50, 1964; Святкина К. А., Хвуль А. М. и Рассолова М. А. Рахит, М., 1964, библиогр.; Тур А. Ф. Рахит, Л., 1966, библиогр.; Усов И. Н. и Станкевич 3. А. Рахит у детей, М., 1980, библиогр.; Фонарев М. И. и Фонарева Т. А. Лечебная физическая культура при детских заболеваниях, Л., 1981; Glissоn F. а. о. De rachitide, sive morbo puerili qui vulgo «the rickets», dicitur, tractatus, L., 1650; Huldschinsky K. Heilung von Rachitis durch kiinstliche Hohensonne, Dtsch. med. Wschr., S. 712, 1919; Stowens D. Pediatric pathology, p. 147, Baltimore, 1966.
Альтернативы костной пластике
Современная стоматология предлагает пациентам обойтись без сложной и не всегда безболезненной процедуры, но альтернатив немного:
Протезирование по схемам: All-on-4 или All-on-6 – недешевые, но крайне эффективные способы восстановить все зубы, даже при сильной атрофии кости. Индивидуально изготовленная челюсть крепится на 4 или 6 опорных штифтов, которые имеют особую конструкцию для быстрейшего приживления и возможности немедленной нагрузки.
Имплантиация All-on-4
- Использование имплантов особой формы – так называемые корневидные импланты разработаны специально для сложных случаев протезирования. Они бывают винтовой или цилиндрической формы, и подбираются исключительно по слепкам и рентгеновским снимкам конкретного пациента.
- Морфогенетический протеин – вводится инъекционно в проблемные участки. Он способствует регенерации тканей, но далеко не всегда эффективен. Ряд исследователей до сих пор относят способ к экспериментальной медицине.
Остеопластика – что это такое, и зачем она нужна?
При внедрении титанового корня очень важно, чтобы он со всех сторон был окружен костью. Если есть дефицит ткани, то титановый штифт будет отторгаться
Более того, если корень установлен в верхнюю челюсть, есть риск задевания верхнечелюстных пазух, что может привести к серьезным ЛОР-заболеваниям. Также при недостатке кости имплантат будет расшатываться, опустится ниже десны, что скажется на эстетике протеза и общей картине.
Остеопластика рекомендована в таких случаях:
- если необходимо установить корень в зону, где свой зуб был удален несколько лет (или месяцев) тому назад;
- если у пациента анатомически большие гайморовые пазухи;
- когда физиологически у человека минимальный объем твердой ткани.
Операция не выполняется, если:
- у пациента хронические ЛОР-заболевания (гаймориты, синуситы, риниты);
- нехватка кальция в организме;
- есть патологии в строении дыхательной системы;
- онкология;
- полипы и другие образования в носу;
- сахарный диабет.
Также остеопластика не выполняется беременным и кормящим женщинам. В остальном, операция делается относительно быстро и с гарантией.
Во многих случаях пациентам перед операцией рекомендуют пропить курс гормональных препаратов и антибиотиков, чтобы нейтрализовать отечные состояния и возможные воспаления.