Мастоциты
Содержание:
Проявления кожных форм
При данной форме поражения затрагивают в основном кожные покровы. При этом основными симптомами являются
- кожный зуд,
- краснота кожи,
- приступы сердцебиений,
- снижение давления,
- периодические подъемы температуры.
Это проявления выхода из тучных клеток особых веществ – гистамина и его аналогов.
Мастоцитоз характеризуется пятью основными типами поражений кожи.
1. Макуло-папулезные проявления. При этом возникают множественные красно-коричневые пятнышки с сильной пигментацией. При проведении особой пробы трением (проба Дарье-Унны) они приобретают вид красных бугорков.
2. Узловой тип – появление внутри кожи множественных шаровидных узлов размерами до 1 см, плотной консистенции красного, розового или желтого цвета. Поверхность узлов гладкая, проба Дарье-Унны отрицательная. Узлы могут сливаться в бляшки.
3. Формирование мастоцитом – единичные узлы размером от 2 до 5 см, гладкие или сморщенные в «апельсиновую корочку», консистенции резины. Может возникать до 3-4 узлов на шее, туловище, предплечьях. Тест Дарье-Унны положительный, а при травмировании поверхности узла на нем могут возникать пузырьки или гнойнички, покалывание. При обратном их развитии кожа над ними западает и морщится.
4. Эритродермическая или диффузная форма — это крупные зудящие очаги коричнево-желтого цвета в области подмышек или ягодичных складок. Они имеют неправильную форму с четкими границами, на ощупь плотные. Поверхность за счет трения может изъязвляться, возникают расчесы и трещины. По мере прогрессирования очаги расползаются, и кожа становится плотной, консистенции теста, цвет ее от розового до темно-коричневого. Тест Дарье-Унны резко положителен, а незначительные травмы очагов дают образование пузырей и зуда. Постепенно процесс регрессирует.
5. Телеагиоэктазийная форма в основном возникает у женщин и проявляется красно-коричневыми пятнами, состоящими из скопления расширенных подкожных сосудов. Эти пятна различной формы и размера, расположены на резко пигментированной кожной основе. На месте их трения возникают волдыри, поражается в основном грудь и конечности, возможен зуд и распространение процесса на кости.
Лечение мастоцитоза
Заболеванием занимаются терапевты и гематологи.
Специфических методов терапии пока не разработано, применяется симптоматическая терапия, подавляющая продуцирование биологически активных веществ тучными клетками:
- антигистаминные средства – супрастин, тавегил, зодак и аналоги.
- стабилизаторы мембран на тучных клетках – недокромил натрия, кетотифен.
- имеются данные об активности альфа-интерферона, но пока метод в стадии разработки.
Применяют также циклоспорины и метилпреднизолон небольшими дозами.
Но пока эффективность лечения невысока.
Применение ПУВА-терапии показано при тяжелом течении мастоцитоза или при устойчивости к противоаллергическим средствам. ПУВА-терапия способствует уменьшению высыпаний. Рекомендуется 25 сеансов по 3-5 Дж/см2 (на сеанс), после чего наблюдается улучшение.
Удаление селезенки показано при диффузном системном мастоцитозе.
Прогнозы при мастоцитозе определяются формой болезни и степенью поражения органов.
При кожной форме он благоприятный, при системной форме может быть различным, а при тучноклеточном лейкозе – крайне неблагоприятный.
Химиотерапевтический метод
Химиотерапия — это применение лекарственных средств, оказывающих повреждающее действие на опухолевую ткань. Чаще всего она является компонентом комплексного лечения и используется как дополнение к хирургическому методу лечения, расширяя его возможности. При некоторых злокачественных опухолях, в частности, при гемобластозах химиотерапия применяется как основной и часто единственный метод лечения. Химиочувствительность опухолевых клеток во многом зависит от особенностей их пролиферации. Активно делящиеся клетки наиболее чувствительны к противоопухолевым воздействиям, а временно или постоянно покоящиеся клетки к ним не чувствительны. Поэтому медленно растущие, высоко дифференцированные новообразования мало чувствительны к химиотерапевтическим воздействиям. Эффективность противоопухолевых препаратов во многом зависит от режима его применения (доза, ритм). Выбор химиопрепаратов, оптимальных доз и интервалов между введениями определяется их фармакокинетикой, гистологическим строением опухоли, её локализацией, а также индивидуальными особенностями организма.
Современная клиническая химиотерапия строится на использовании повторных курсов комбинаций противоопухолевых препаратов.
Дозирование химиотерапевтических препаратов
Дозировку каждого химиотерапевтического препарата необходимо подбирать таким образом, чтобы препарат оказывал цитотоксическое действие на клетки опухоли, при этом минимально повреждая клетки здоровых тканей. Как правило, медицинские дозировки не применимы для животных это связанно в первую очередь с невозможностью контроля тяжелых токсикозов и побочных эффектов, вызываемых высокими дозировками. Дозировку большинства химиотерапевтических препаратов рассчитывают относительно площади поверхности тела, а не относительно веса. Это связанно с тем, что кровоток через внутренние органы, в первую очередь через печень и почки, зависит больше от площади поверхности тела, чем от веса.
Зависимость площади поверхности тела от веса
Осложнения химиотерапии
Клиницист должен четко осознавать потенциальную токсичность химиотерапевтических препаратов, особенно для пациентов с сопутствующими заболеваниями, и внимательно следить за ходом лечения. Для этого необходимо до начала лечения оценить состояние внутренних органов, в первую очередь сердца печени и почек, состояние кроветворения, уровни гемоглобина, эритроцитов, лейкоцитов, лимфоцитов. На практике непосредственно перед проведением курса химиотерапии необходимо провести гематологический и биохимический анализы крови, снять кардиограмму. В дальнейшем для контроля возможных осложнений и своевременного купирования побочных эффектов необходимо проводить гематологический анализ один раз в неделю, биохимический — один раз в три — четыре недели. В связи с тем, что химиопрепараты обладают малой избирательностью действия и повреждает любую быстро растущую ткань, осложнения чаще всего наблюдаются со стороны органов и тканей содержащих большое количество делящихся клеток.
Непосредственно после введения химиотерапевтических препаратов наиболее распространенным осложнением является рвота.Онанаиболее характерна после введения препаратов платины и доксорубицина. В большинстве случаев рвоту можно купировать предварительным ведением противорвотных препаратов (церукал, торекан, ондансетрон и новобан) в комбинации с кортикостероидами, а также снижением скорости инфузии химиотерапевтических препаратов.
Следующим по частоте встречаемых осложнений является диарея. Для купирования данного осложнения необходимо назначение спазмолитиков, препаратов висмута, и антибиотиков и инфузионной терапии. Наиболее распространенное осложнение, присущее в той или иной степени всем цитостатикам (за исключением винкристина и блеомицетина), — возникающая через несколько дней после введения препаратов — миелосупрессия. Связанно это с тем, что химиотерапевтические препараты поражают костный мозг. Могут быть подавлены все предшественники лейкоцитов, тромбоцитов и эритроцитов, что приводит к лейкопении, тромбоцитопении и анемии. Основными последствиями тяжелой гранулоцитопении является риск инфекционных осложнений. Поэтому, при снижении гранулоцитов менее 3 — 4 тыс. в мл., необходимо назначение антибиотиков широкого спектра действия. С анемией борются назначением препаратов железа и эритропоэтинов. На практике, после проведения цикла химиотерапии, проводится инфузионная терапия в течение 5 — 7 дней, и контроль гематологических показателей, что позволяет предупреждать возникновение острых осложнений.
Как диагностировать опухоль
Конкретных проявлений, которые характеризуют новообразования, практически нет, однако они легко поддаются диагностике при помощи биопсии. Для взятия материала используется тонкая игла, поэтому собака практически не ощущает боли. Изъятые материалы отправляются в лабораторию для досконального изучения.
Клетки, из которых состоит мастоцитома, большие и круглые. Они содержат вещества, которые могут стать причиной рвоты, язвы желудка, шока и привести к летальному исходу.

Мастоцитомные клетки имеют очень непредсказуемый характер. Даже сегодня нет стопроцентной возможности отличить опухоли, которые будут протекать агрессивно, рецидивировать, метастазировать или приведут к смерти от излечимых опухолей.
Достаточно точно диагностируют онкозаболевания в клинике «Биоконтроль». Ветклиника специализируется на таких заболеваниях и располагает необходимым оборудованием.
Для того чтобы определить прогноз заболевания, нужно правильно выявить степень дифференциации образования, которая покажет, насколько злокачественные клетки отличны от доброкачественных и какова вероятность излечения.
Симптоматика заболевания
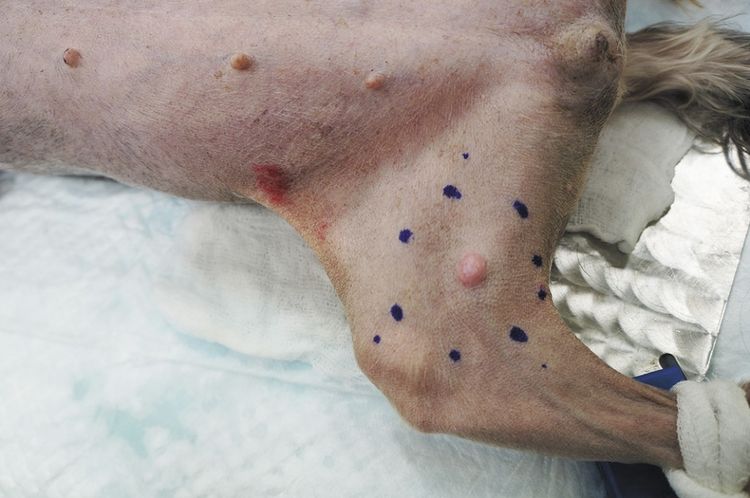
Один из первых признаков мастоцитомы – образование на коже, напоминающее родинку, папиллому или бородавку, на месте появления которого возможно выпадение шерстного покрова. Чаще всего оно появляется в области живота, на конечностях, реже – на шее, голове, половых органах. На первых этапах опухоль характеризуется зачастую медленным темпом роста (при единичных образованиях) и зачастую не доставляет беспокойства животному. Она может иметь расплывчатый или ограниченный контур, мягкую или твердую консистенцию, окрас отрозового до темно-вишневого цвета или быть без особого окраса. Появление следующих симптомов у собаки должно стать поводом для незамедлительного обращения в ветклинику:
- Сильный зуд, вынуждающий пса расчесывать, разгрызать место поражения.
- Покраснения, отеки, воспалительные процессы в месте опухоли.
- Эрозии и язвы области образования.
- Образование папул и пустул величиной от нескольких миллиметров до 4-5 см.
- Сопутствующие нарушения здоровья (рвота, следы крови в кале) и заболевания (язва двенадцатиперстной кишки, нарушение свертываемости крови).
Важно! Один из опасных симптомов мастоцитомы – синдром Дарье. Если при растирании самого образования и окружающей кожи рядом образуются красные узелки, это говорит об агрессивной стадии развития
Из-за разнообразных симптомов ветеринары часто называют мастоцитомы «имитаторами», поскольку они могут замаскироваться на первых этапах под стандартную аллергическую реакцию. Новообразования могут иметь злокачественную или доброкачественную природу, причем рядом могут развиваться опухоли разной этиологии.
Клиническое значение
Паразитарные инфекции
Тучные клетки активируются в ответ на инфекцию патогенными паразитами, такими как определенные гельминты и простейшие , посредством передачи сигналов IgE .
Нарушения активации тучных клеток
Расстройства активации тучных клеток ( MCAD ) представляют собой спектр иммунных нарушений , которые не связаны с патогенной инфекцией и включают аналогичные симптомы, которые возникают из-за секретируемых промежуточных продуктов тучных клеток, но немного отличаются по своей патофизиологии , подходу к лечению и отличительным симптомам. Классификация нарушений активации тучных клеток была заложена в 2010 году.
Аллергическая болезнь
Аллергия передается через передачу сигналов IgE, которая запускает дегрануляцию тучных клеток.
Многие формы кожной и слизистой аллергии в значительной степени опосредованы тучными клетками; они играют центральную роль при астме , экземе , зуде (по разным причинам), аллергическом рините и аллергическом конъюнктивите . Антигистаминные препараты действуют, блокируя действие гистамина на нервные окончания. Лекарства на основе кромогликата (кромогликат натрия, недокромил) блокируют кальциевый канал, необходимый для дегрануляции тучных клеток, стабилизации клетки и предотвращения высвобождения гистамина и родственных медиаторов. Антагонисты лейкотриенов (такие как монтелукаст и зафирлукаст ) блокируют действие медиаторов лейкотриена и все чаще используются при аллергических заболеваниях.
Кальций вызывает секрецию гистамина тучными клетками после предыдущего воздействия фторида натрия. Секреторный процесс можно разделить на стадию активации фторидом и секреторную стадию, индуцированную кальцием. Было замечено, что стадия активации фтором сопровождается повышением уровней циклического аденозинмонофосфата (цАМФ) в клетках. Достигнутые высокие уровни цАМФ сохраняются во время высвобождения гистамина. Кроме того, было обнаружено, что катехоламины существенно не изменяют индуцированное фторидом высвобождение гистамина. Было также подтверждено, что вторая, но не первая стадия индуцированной фторидом натрия секреции гистамина ингибируется теофиллином. Расширение сосудов и повышенная проницаемость капилляров являются результатом действия рецепторов как H1, так и H2.
Стимуляция гистамина активирует аденилатциклазу кислородных клеток, чувствительную к гистамину (Н2), и происходит быстрое увеличение клеточного , которое участвует в активации транспорта Н + и других связанных изменениях оксинтических клеток.
Анафилаксия
При анафилаксии (тяжелая системная реакция на аллергены , такие как орехи, укусы пчел или лекарства) дегрануляция тучных клеток на всем теле приводит к расширению сосудов и, в тяжелых случаях, к симптомам опасного для жизни шока .
Гистамин — это сосудорасширяющее вещество, выделяющееся во время анафилаксии.
Аутоиммунитет
Тучные клетки могут быть вовлечены в патологию, связанную с аутоиммунными воспалительными заболеваниями суставов. Было показано, что они участвуют в рекрутировании воспалительных клеток в суставы (например, ревматоидный артрит ) и кожу (например, буллезный пемфигоид ), и эта активность зависит от антител и компонентов комплемента.
Мастоцитоз и клональные нарушения
Мастоцитоз — редкое заболевание клональных тучных клеток, включающее присутствие слишком большого количества тучных клеток ( мастоцитов ) и предшественников тучных клеток CD34 +. Мутации в c-Kit связаны с мастоцитозом.
Неопластические расстройства
Мастоцитомы или опухоли тучных клеток могут секретировать чрезмерное количество продуктов дегрануляции. Их часто можно увидеть у собак и кошек. Другие опухолевые расстройства , связанные с тучными клетками , включают тучные клетки саркому и тучные клетки лейкемию .
Синдром активации тучных клеток
Синдром активации тучных клеток (MCAS) — это идиопатическое иммунное заболевание, которое включает повторяющуюся и чрезмерную дегрануляцию тучных клеток и вызывает симптомы, сходные с другими нарушениями активации тучных клеток. Синдром диагностируется на основе четырех наборов критериев, включающих ответ на лечение, симптомы, дифференциальный диагноз и биомаркеры дегрануляции тучных клеток.
Активация
Схема строения рецептора FcεR1
FcεR1 представляет собой высокоаффинный рецептор IgE на поверхности тучных клеток. FcεR1 — тетрамер из одной α-, одной β- и двух γ-цепей, соединённых дисульфидными мостиками. Сайт связывания IgE сформирован внеклеточной частью α-цепи, содержащей два домена, близких к иммуноглобулиновым. В состав β-цепи и каждой из двух γ-цепей входит активирующий мотив ITAM. Активирующий сигнальный каскад на FcεR1 запускается, когда ITAM в составе β- и γ-цепей фосфорилируются по остаткам тирозина.
Схема активации тучной клетки
Сигнальный путь, активирующийся при кросс-связывании FcεR1 с аллергеном при участии IgE, очень похож на тот, который запускается при активации лимфоцитов антигенами. С цитоплазматической частью β-цепи FcεR1 связана тирозинкиназа Lyn, и после кросс-связывания FcεR1 с аллергеном она фосфорилирует мотивы ITAM в β- и γ-цепях FcεR1. Другая тирозинкиназа, Syk, связывается с фосфорилированными ITAM в γ-цепях и активируется, фосфорилируя множество других белков и активируя их, тем самым увеличивая сигнал.
Среди белков, активируемых Syk, особенно важен белок LAT, который в результате фосфорилирования приобретает способность к взаимодействию со многими белками. В частности, фосфолипаза C гамма (PLCγ) активируется в результате связывания с LAT и катализирует расщепление фосфатидилинозитол-4,5-бисфосфата на инозитолтрифосфат (IP3) и диацилглицерин (DAG). IP3 повышает уровень ионов кальция в цитозоле, а DAG активирует протеинкиназу C (PKC). PKC фосфорилирует лёгкие цепи миозина, из-за чего базофильные гранулы приходят в движение и достигают контакта с клеточной мембраной. Далее гранула сливается с мембраной при участии белков SNARE, высвобождая наружу своё содержимое.
Активированные тучные клетки синтезируют и выделяют эйкозаноиды и цитокины. Среди эйкозаноидов в тучных клетках наиболее активно синтезируются лейкотриен C4 и {{нп5|простагландин E2||en|Prostaglandin E2]}. Образование эйкозаноидов контролирует цитозольный фермент фосфолипаза A2, который активируется при повышении концентрации кальция в цитозоле или фосфорилировании.
По спектру выделяемых цитокинов тучные клетки близки к T-хелперам 2 типа, или Th2-клеткам. Они продуцируют такие цитокины, как IL-3, IL-4, IL-5, IL-6, IL-10, IL-13, GM-CSF, а также провоспалительные цитокины IL-1, IL-8, IL-12, IL-18, IL-21, IL-23, TNF-α и гомеостатические цитокины IL-7 и IL-15. Также они вырабатывают TGFβ, ряд хемокинов и интерфероны основных типов. Большинство цитокинов тучные клетки синтезируют под действием внешних стимуляторов, и лишь IL-4, TNF и GM-CSF они выделяют постоянно. Кроме того, активированные мастоциты продуцируют ряд ростовых факторов: фактор роста эндотелия сосудов (VEGF), фактор роста фибробластов (FGF) и фактор роста нервов (NGF).
Как мастоцитома у собаки реагирует на химиотерапию
При типичном режиме химиотерапии назначается «Преднизолон», дозировка которого рассчитывается в зависимости от веса животного. После двухнедельного приема препарата проверяют результаты. И если положительного эффекта не выявлено, то назначается следующий протокол химиотерапии, который состоит из «Циклофосфана», «Винбластина» и «Преднизолона».
«Преднизолон» наиболее часто применяется при мастоцитомах. Животные хорошо его переносят и продолжительность приема может длиться полгода. Если во время лечения новых опухолей выявлено не было, то лекарство, возможно, отменят.
При приеме препарата может увеличиваться масса тела, повышаться аппетит и жажда, могут наблюдаться инфекционные поражения кожных покровов и одышка. Реже можно наблюдать расстройство желудка, язвенные болезни и панкреатит. Если такие симптомы имеют место, то назначается дополнительная терапия, направленная на уменьшение побочных эффектов.
Если опухоль располагается в труднодоступных местах или ее невозможно удалить, то применяется комбинированная химиотерапия. Она тормозит рост опухоли и ее распространение по организму на протяжении длительного времени, которое может исчисляться неделями, месяцами и годами. Полное уничтожение тучноклеточной опухоли невозможно, но некоторые животные смогут прожить еще несколько лет и достичь биологической старости.
Патогенез
Тучные клетки были так названы в связи с наличием особо окрашивающихся крупных базофильных гранул (поэтому еще называются тканевыми базофилами) с гистамином и гепарином. Мастоциты были впервые описаны в 1878 г. Эрлихом, который ошибочно предположил, что они служат для питания окружающих тканей и назвал «Mastzellen» (термин происходит от немецкого слова Mast — «откармливание» животных). Однако, сегодня уже известно, что мастоциты являются очень мощными клетками иммунной системы, участвующими в воспалительных процессах в частности при активации IgE-опосредованных механизмов за счет высвобождения различных медиаторов и воспалительных цитокинов, триптазы, гистамина, серотонина, гепарина, тромбоксана, простагландина D2, лейкотриена C4, факторов активации тромбоцитов, факторов хемотаксиса эозинофилов и интерлейкинов. В случае эпизодического спонтанного высвобождения медиаторов и развивается симптоматика мастоцитоза.
Залегают тучные клетки практически во всех органах, близко располагаясь к сосудам кровеносной и лимфатической системы, эпителиальным поверхностям и периферическим нервам, поэтому они способны выполнять различные регуляторные и защитные функции. Развитие тучных клеток начинается с плюрипотентных клеток-предшественников в костном мозге, которые рассеиваются и подвергаются пролиферации, а затем созревают в определенных тканях в результате взаимодействия факторов роста, цитокинов и экспрессии рецепторов типа c-KIT. Фактор роста и пролиферации тучных клеток дополнительно стимулирует процесс разрастания меланоцитов и образования меланина, что в результате приводит к гиперпигментации и особым мастоцитозным высыпаниям на коже.
При гиперпролиферации мастоцитов развивается реактивная гиперплазия либо опухолевый процесс. Стимулировать неупорядоченную клональную пролиферацию предположительно могут нарушения в рецепторах c-KIT (чаще мутации, вызывающие усиление экспрессии) и гиперпродукция лигандов.
Стимулировать проявление мастоцитоза в любом возрасте – при рождении или по достижении зрелости могут некоторые фармакологические и физические раздражители (тепло, холод или давление), вызывающие дегрануляцию тучных клеток и выделение простагландинов, гистамина, лейкотриенов и прочих медиаторов. Такие эпизодические атаки вызывают гиперемию кожи и крапивницу, а в самых тяжелых случаях — коллапс с угрозой для жизни больного.
Дегрануляция тучной клетки по D.Lawson
Описание
Гистамин — маркер развития опухолевого процесса ряда опухолей желудка, тонкой кишки, двенадцатиперстной кишки (карциноидов — опухолей, продуцирующих гистамин).
Гистамин — это биогенный амин, который выполняет роль нейротрансмиттера (то есть вещества, передающего импульс) в центральной нервной системе. Гистамин является медиатором различных локальных нервных реакций, в частности, он участвует в регуляции тонуса гладкой мускулатуры матки, сосудов, кишечника, регулирует секрецию кислоты в желудке, именно гистамин является патогенетическим компонентом ряда патологических реакций. Гистамин — первый иденцифицированый медиатор аллергии, синтезирующийся в тучных клетках.Биологические эффекты гистамина
По механизму действия на кровеносные сосуды он резко отличается от других биогенных аминов, так как обладает сосудорасширяющим свойством. Он способствует повышению проницаемости капилляров, вызывает сокращение гладкой мускулатуры матки. Большое количество гистамина образуется в области воспаления, что имеет определенный биологический смысл. Вызывая расширение сосудов в очаге воспаления, гистамин тем самым ускоряет приток лейкоцитов, способствуя активации защитных сил организма. Кроме того, гистамин участвует в секреции соляной кислоты в желудке, что используется в клинике при исследовании секреторной деятельности желудка (гистаминовая проба). Он имеет прямое отношение к явлениям сенсибилизации и десенсибилизации. Гистамин постоянно образуется в различных органах и тканях. Большое количество гистамина секретируется тучными клетками (в клетках соединительной ткани) и базофилами (в клетках крови).
Гистамин стимулирует гладкие мышцы кишечника, что может сопровождаться диареей при анафилактических реакциях. При повышенной чувствительности к гистамину в клинике используют антигистаминные препараты (санорин, димедрол и другие), оказывающие влияние на рецепторы сосудов. Гистамину приписывают также роль медиатора боли. Болевой синдром — сложный процесс, детали которого пока не выяснены, но участие в нем гистамина не подлежит сомнению.Гистамин в лабораторной диагностике
В лабораторной диагностике исследование гистамина используют в диагностике анафилактических реакций. Уровень гистамина растет в течение 5–10 минут от начала приступа, снижаясь до базального уровня в течение следующих 30–60 минут. Во время асимптоматичного периода уровень гистамина у таких пациентов находится в пределах нормы.
Исследование гистамина представляет интерес в диагностике карциноидных опухолей, хотя этот тест имеет меньшее значение, чем исследование метаболитов серотонина.
Содержание гистамина плазмы повышено у пациентов с мастоцитозом, тест можно использовать в комплексной оценке состояния таких пациентов, но он не является диагностическим для данной патологии. Показания:
- дифференциальная диагностика анафилактических реакций (подтверждение аллергической природы);
- мастоцитоз, оценка состояния пациентов;
- в комплексе обследований при подозрении на карциноидные опухоли.
Подготовка
Кровь рекомендуется сдавать утром, в период с 8 до 12 часов. Взятие крови производится натощак или спустя 6–8 часов голодания. Допускается употребление воды без газа и сахара. Накануне сдачи исследования следует избегать пищевых перегрузок.Интерпретация результатов
Единицы измерения: нмоль/л.
Референсные значения: <9.3 нмоль/л. Повышение:
- аллергический ответ (анафилаксия);
- карциноидные опухоли;
- миелопролиферативные неоплазмы;
- мастоцитоз.
5 стадий развития рака
Излечимость рака напрямую зависит от того, на какой стадии развития он находится. В практической онкологии при определении тяжести процесса принято ориентироваться на международную классификацию TNM. Расшифровка аббревиатуры простая:
- T – это характеристика первичной опухоли. В зависимости от ее размера определяется стадия T1-T4.
- N – это метастазы в региональных лимфатических узлах. По степени вовлеченности лимфоузлов выделяют стадии N1-N3.
- M – это отдаленные метастазы – проникновение клеток опухоли в другие органы. M0 ставится, если метастазов нет, M1 – при их наличии вне зависимости от количества и локализации.
В зависимости от параметров T,N и M определяется стадия развития болезни. Рассмотрим подробнее, как лечится рак на различных этапах и какова вероятность благополучного исхода.
0 стадия
Стадия 0 – это рак in situ, или рак на месте. Опухоль располагается в пределах эпителиальной ткани (слизистой оболочки) и не переходит в более глубокие слои. В этой стадии клетки новообразования растут с той же скоростью, что и гибнут. Не прорастают сосуды в злокачественные ткани, не отсеиваются раковые клетки в лимфатические узлы. Симптомов заболевания нет. До начала активного роста проходит несколько лет или даже десятилетий. Выявить рак in situ можно только при обследовании (например, при прохождении планового медицинского осмотра).
Рак 0 стадии полностью излечим – достаточно избавиться от очага измененных тканей. Операция малоинвазивная, с минимальным повреждением органа. Прогноз благоприятный – после хирургического вмешательства рак не рецидивирует. По статистике, чаще всего такие формы опухолей выявляются на шейке матки, кожных покровах – там, где они доступны для визуального осмотра и/или скринингового исследования.
I стадия
В стадии I выявляется небольшая первичная опухоль. У каждой формы патологии определяются свои допустимые размеры. Например, для молочной железы это образование до 2 см, а для меланомы (опухоли кожи) – всего 2 мм. Регионарные лимфоузлы не поражены.
I стадия – это самая благоприятная стадия рака. Нужно только полностью убрать первичный очаг – удалить подозрительное образование на коже, сегмент молочной железы и т. п. Пятилетняя выживаемость доходит до 100%. Практически все пациенты, прошедшие лечение вовремя, полностью выздоравливают. Но если болезнь не лечить, она будет прогрессировать. Рак перейдет во вторую стадию с дальнейшим поражением тканей и лимфатических узлов.
II стадия
Во II стадии первичная опухоль растет. Например, образование молочной железы достигает величины 5 см, кожи – до 4 мм. В некоторых регионарных лимфатических узлах выявляются раковые клетки. Процесс выходит за пределы первичного очага.
Пятилетняя выживаемость на этой стадии развития рака составляет 50-80%. Рак можно излечить только в том случае, если полностью избавиться от первичного очага и убрать пораженные лимфатические узлы. Для закрепления результата нередко проводится химиотерапия, лучевое облучение.
III стадия
В стадии III опухоль достигает больших размеров. В регионарных лимфоузлах определяются раковые клетки. Обычно на этой стадии поражается несколько лимфатических узлов. Отдаленных метастазов еще нет, соседние органы не изменены.
Рак III степени возможно вылечить, если помощь будет оказана вовремя. Требуется комплексный подход – нужно не только убрать первичный очаг и измененные лимфатические узлы, но и предупредить распространение атипичных клеток по организму. Для этого ткани облучают, вводят цитостатические препараты, способные уничтожить раковую опухоль. Пятилетняя выживаемость на этой стадии составляет 30-50%.
IV стадия
Стадия IV – самый тяжелый вид раковой опухоли. Здесь появляются метастазы, и атипичные клетки распространяются в другие органы. Например, при раке молочной железы новые очаги обнаруживаются в костях, легких, головном мозге и печени. Размер первичной опухоли не имеет значения. Распространение метастазов возможно даже при маленьких образованиях.
Пятилетняя выживаемость в последней стадии рака невысока и составляет не более 10%. Рак с метастазами практически не излечим. Для удаления опухоли требуются обширные травматичные операции, курсы химиотерапии и лучевого облучения. Не всякий организм выдерживает подобную нагрузку.
Важно! Чем быстрее будет обнаружена злокачественная опухоль, тем выше шансы на выздоровление. Рак на ранних стадиях практически всегда излечим
Своевременная диагностика и грамотное лечение позволяют полностью избавиться от опасной болезни и избежать развития осложнений.
Опухоли кожи
Это довольно разнообразная в морфологическом отношении группа,составляющая значительную часть новообразований у животных, к которой относят опухоли эпителиального происхождения, нейроэктодермального (невусы, меланомы) и мезенхимального происхождения (см. опухоли мягких тканей).
Доброкачественные опухоли кожи
Самыми распространенными доброкачественными опухолями кожи являются:
- папилломы;
- невусы;
- эпидермальные кисты;
- аденомы придатков кожи;
- аденома гепатоидных желез;
- гемангиомы;
- гистиоцитома.
Злокачественные опухоли кожи
- плоскоклеточный рак;
- базалиома;
- рак придатков кожи;
- кератоакантома;
- меланома;
- гепатоидная аденокарцинома.
Выделяют следующие клинические стадии рака кожи (ВОЗ, 1980г.):
- Т-преивазивная карцинома;
- Т-0 первичная опухоль не определяется;
- Т-1 опухоль менее 2 см в максимальном диаметре, поверхностно расположенная, эндофитная или экзофитная;
- Т-2 опухоль от 2 до 5 см в максимальном диаметре или с минимальной инфильтрацией дермы, независимо от размера;
- Т-3 опухоль больше 5 см в максимальном диаметре или с инфильтрацией подкожной клетчатке независимо от размеров;
- Т-4 опухоль, инфильтрирующая в другие структуры (фасции, мышцы, кость или хрящ).
- N-0 лимфатические узлы не пальпируются.
- N-1 подвижные лимфатические узлы на стороне поражения ( 1а — лимфатические узлы не увеличены, 1б — лимфатические узлы увеличены).
- N-2 подвижные лимфатические узлы на противоположной стороне или с двух сторон (2а — лимфатические узлы не увеличены, 2б — лимфатические узлы увеличены).
- N-3 неподвижные лимфатические узлы с любой стороны или с обеих сторон.
- М-0 нет выявленных метастазов.
- М-1 отдаленные метастазы.
Плоскоклеточный рак
По гистологическому строению может быть с ороговением и без ороговения. Ороговевающий рак более дифференцированный. Опухолевый процесс может протекать в виде язвенной или узловатой формы и локализоваться на любом участке тела. К характерным признакам относят образование язвы с приподнятыми валикообразными краями инфильтрата или массивного узла. Более злокачественное течение с тенденцией к прорастанию в подлежащие ткани и метастазированию в региональные лимфатические узлы свойственно раку с локализацией на кожно-слизистых стыках, лапах, предплечье и голени.
Базалиома
Опухоль в основном локализуется на коже головы, шеи, конечностей, реже туловище. Базалиома может быть в виде уплотненной плоской бляшки, бородавчатого разрастания, почти все формы склонны изъязвляться. После радикального удаления склонны рецидивировать. Метастазирует поздно при значительных размерах.
Кератоакантома
Условно-доброкачественная опухоль, обладает местно-деструктивным ростом, может врастать в кость и надкостницу. Не метастазирует.
Меланома
Кожные меланомы встречаются реже, чем меланомы полости рта. В основном они расположены на дистальной части конечности или кожно-слизистых соединениях (губы, веки), где они имеют очень злокачественную природу. Чисто кожные меланомы — условно-доброкачественны. Характерными чертами являются изъязвление и вторичные инфекции. Уже на ранних стадиях наблюдаются региональные и отдаленные метастазы.
Диагноз
Диагностика злокачественных опухолей кожи основана на клинических данных и подтверждается гистологическими и цитологическими исследованиями.
Лечение
Для лечения опухолей кожи необходимо радикальное удаление с захватом не менее 1 см окружающих тканей. При мастоцитомах не менее 3х см. При локализованных процессах возможно применение криодеструкции и цитостатические мази (проспидиновая, колхаминовая и др.). При удалении злокачественных меланом захват здоровых тканей должен быть не менее 3 см от края опухоли. Для лечения местно-распространенных и метастазирующих опухолей возможно применить химиотерапию по схеме:
- Доксорубицин 40 мг на метр квадратный в первый день.
- Цисплатин 40 мг на метр квадратный в первый день
Каждые 3 -4 недели. На курс — 6 циклов.
После удаления злокачественных меланом необходимо применить химиотерапию по схеме:
- Доксорубицин 40 мг на метр квадратный в первый день.
- Дакарбазин 150 мг на метр квадратный с 1-го по 5-й день.
Каждые 3 -4 недели. На курс — 6 циклов