Гипокортицизм
Содержание:
Литература
- Фадеев В.В. Мельниченко Г.А. Надпочечниковая недостаточность. РМЖ. 2001; 24: 1088–1095.
- Федеральные клинические рекомендации (протоколы) по ведению детей с эндокринными заболеваниями. Под ред. И.И. Дедова, В.А. Петерковой. М.: Практика, 2014.
- Эндокринология. Национальное руководство. Краткое издание. Под ред. И.И. Дедова, Г.А. Мельниченко. М.: ГЕОТАР-Медиа, 2011.
- Henderson K. The Washington Manual Endocrinology. Lippincott: Willisms & Wilkins, 2004.
- Bornstein S.R., Allolio B., Arlt W., et al. Diagnosis and treatment of primary adrenal insufficiency: an endocrine society clinical practice guideline. J. Clin. Endocrinol. Metab. 2016; 101(2): 364–389. DOI: 10.1210/jc.2015-1710
- Greenspan T.S., Gardener D. Basic and clinical endocrinology. McGraw-Hill, 2004.
- Boumpas D.T., Chrousos G.P., Wilder R., et al. Glucocorticoid therapy for immune-mediated diseases: basic and clinical correlates. Ann. Intern. Med. 1993; 119(12): 1198–1208.
- Savage M.W., Mah P.M., Weetman A.P., Newell-Price J. Endocrine emergencies. Postgrad. Med. J. 2004; 80(947): 506–515.
- Besser G.M., Thorner M.O. Comprehensive clinical endocrinology. Edinburgh: Elsevier Science, 2002.
- Интенсивная терапия. Национальное руководство. Краткое издание. Под ред. Б.Р. Гельфанда, И.Б. Заболотских. 2-е изд., перераб. и доп. М.: ГЭОТАР-Медиа, 2019.
- Окороков А.Н. Неотложная эндокринология. М.: Мед. лит., 2011.
- Потемкин В.В., Старостина Е.Г. Неотложная эндокринология. Руководство для врачей. М.: Медицинское информационное агентство, 2008.
- Becker K.L., Bilezikian J.P., Bremner W.J., et al. Principles & Practice Endocrinology & Metabolism. Lippincott: Williams & Wilkins, 2002.
- Hamrahian A.H., Roman S., Milan S., et al. The management of the surgical patient taking glucocorticoids. Edited by UpToDate. Available at: http://www.uptodate.com/contents/the-surgical-patient-taking-glucocorticoids. Accessed December 10, 2015.
- Периоперационное ведение пациентов с сопутствующими заболеваниями. Руководство для врачей. Под ред. И.Б. Заболотских. М.: Практическая медицина, 2019.
- Неотложная эндокринология. Учебное пособие. Л.А. Жукова, С.А. Сумин, Т.Ю. Лебедев и др. М.: Медицинское информационное агентство, 2006.
- Fleisher L.A. Mythen M. Anesthetic implications of concurrent diseases. In: Miller R.D., Eriksson L., Fleisher L., et al. Millerʼs Anesthesia. 8th ed. Vol. 1. Philadelphia: Elsevier Churchill Livingstone, 2015: 1172–1174.
- «Анестезия» Рональда Миллера. Под ред. Р. Миллера. Пер. с англ. под общей ред. К.М. Лебединского: в 4 т. СПб.: Человек, 2015. Т. 2. С. 1139–1235. DOI: 10.1097/ALN.0000000000001659
- Liu M.M., Reidy A.B, Saatee S., Collard C.D. Perioperative steroid management: approaches based on current evidence. Anesthesiology. 2017; 127(1): 166–172. (In Russ)]
- Schwartz J.J., Akhtar S., Rosenbaum S.H., et al. Endocrine Function. In: Clinical Anesthesia. Barash P.G., Cullen B.F., Stoelting R.K., et al. 7th ed. Edited by Philadelphia, Wolters Kluwer/Lippincott Williams & Wilkins, 2013: 1137–1138.
- Wall R.T. III. Endocrine disease. In: Stoeltingʼs anesthesia and co-existing disease. 7th ed. Hines R., Marschall K. Philadelphia, Saunders/Elsevier, 2017: 449–477.
Диагностика
Клиническими критериями подтверждения гипокортицизма являются: характерная пигментация кожи, снижение веса тела, нехарактерная реакция на физическую нагрузку (понижение артериального давления), уменьшение кортизола в крови (менее 100 нмоль/л), повышение количества калия в крови (свыше 5 ммоль/л), снижение натрия в сыворотке крови (менее 230 ммоль/л), гипогликемия. Кортикотропин при первичном гипокортицизме имеет тенденцию к нарастанию свыше 100 нмоль/л и снижается при вторичном.
На начальных стадиях заболевания с целью уточнения диагноза проводится функциональная проба аналогом кортикотропина продолжительного действия синактеном-депо. В случае первичного гипокортицизма заболевание характеризуется отсутствием нарастания кортизола в крови после проведенной стимуляции, при вторичном гипокортицизме концентрация кортизола явно возрастает.
Дифференциальная диагностика
Заболевание необходимо дифференцировать от состояний, которые могут сопровождаться гиперпигментацией кожи, общим недомоганием, снижением веса тела, устойчивой гипотензией: диффузный токсический зоб, гиперхроматоз, хронические поражения кишечника, невротические синдромы.
Диагностика и лечение
Для диагностики острой надпочечниковой недостаточности назначают:
- Общий анализ крови. Отмечается повышение количества эритроцитов (эритроцитоз) и гемоглобина (за счет сгущения крови), увеличение количества лейкоцитов и СОЭ;
- Анализ крови на сахар: гипогликемия (снижение уровня сахара);
- Биохимический анализ крови: отмечается повышение уровня калия и креатинина, снижение уровня натрия, хлоридов;
- Общий анализ мочи: определяется белок, эритроциты, иногда ацетон;
- Исследование уровня гормонов надпочечников в моче и в крови: выявляется резкое снижение количества кортикостероидов (кортизола, альдостерона и др.);
- ЭКГ: признаки гиперкалиемии.
Лечение проводится в отделении реанимации или интенсивной терапии.
Основа лечения — капельницы с кортикостероидами и специальными растворами. Также проводятся мероприятия по выведению больного из шокового состояния. Если лечение начато вовремя, шансы вывести больного из криза повышаются.
После выздоровления у больных остаются признаки нарушения функции надпочечников, поэтому они нуждаются в пожизненной заместительной терапии синтетическими аналогами гормонов коры надпочечников.
Когда женщина превращается в мужчину …
Андростерома — опухоль коры надпочечника, продуцирующая избыточное количество андрогенов. Эти достаточно редкие опухоли (1-3% всех новообразований надпочечников) выявляются во всех возрастных группах, но преимущественно у женщин в возрасте до 40 лет. Редкость обнаружения андростером у мужчин может быть связана с меньшей отчетливостью у них признаков вирилизации; часть этих новообразований имитирует гормонально-неактивные опухоли надпочечников.
Симптоматика при андростероме характеризуется быстрой вирилизацией. У девочек отмечаются рост волос на лобке по мужскому типу, увеличение клитора в пубертатный период, отсутствие роста молочных желез и менструаций, усиленное развитие мускулатуры, появление мужского тембра голоса. У мальчиков наблюдаются признаки преждевременного полового созревания.
У женщин уменьшается подкожный жировой слой, становится более рельефной мускулатура, увеличивается ее масса, грубеет и становится низким голос. Наблюдается рост волос на лице, теле и конечностях, выпадают волосы на голове. Менструации вскоре прекращаются. Уменьшаются молочные железы. Значительно увеличивается клитор. В большинстве случаев отмечается повышенное либидо.
Решающее значение при постановке диагноза андростеромы имеют данные КТ и МРТ. УЗИ помогает выяснить топографические взаимоотношения опухоли с почкой, аортой, нижней полой веной, селезенкой и печенью, что необходимо для выбора оперативной тактики.
Лечение андростером только оперативное — удаление пораженного опухолью надпочечника. В случае успешного удаления опухоли симптомы заболевания довольно быстро подвергаются обратному развитию. В запущенных случаях и у пациентов с неоперабельными опухолями или отдаленными метастазами лечение симптоматическое.
Прогноз при ранней диагностике и своевременном оперативном лечении доброкачественных андростером благоприятный. Однако довольно часто дети остаются низкорослыми вследствие раннего закрытия зон роста. При злокачественных андростеромах и наличии отдаленных метастазов прогноз неблагоприятный.
Симптоматическая картина
И для первого, и для второго типа заболевания характерна практически идентичная картина симптоматических проявлений:
- отсутствие аппетита, в результате чего масса тела может снижаться до критических отметок. Следует также отметить, что на фоне общего снижения аппетита наблюдается патологическая тяга к соленой пище;
- общая усталость и ослабление мышц, которое носит быстро прогрессирующий характер;
- снижение артериального давления, которое сопровождается потерей сознания и головокружением;
- нарушения в работе желудочно-кишечного тракта: боли в желудке, рвота, диарея или запор;
- нервно-психологические нарушения: вялость, беспричинная раздражительность, апатия, отсутствие сексуального влечения и др.;
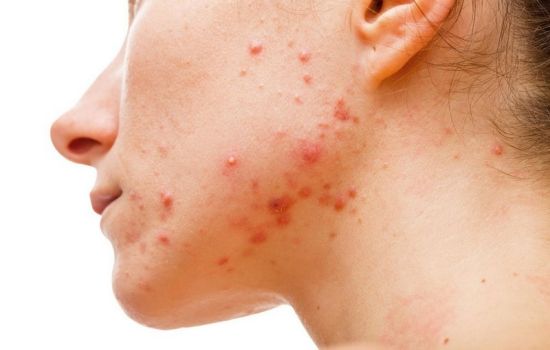
- пигментация кожных покровов (специфический симптом первичной патологии) изначально напоминает обычный загар и появляется, прежде всего, на участках тела, которые подвержены солнечному облучению (лицо, руки, шея, ноги). Однако с развитием заболевания «загар» приобретает нездоровый цвет и появляется на скрытых участках (грудь, внешние половые органы, анус, подмышки и т.д.). Еще позже появляются пигментные пятна сине-черного цвета на слизистых оболочках (ротовая полость, влагалище).
Симптомы опухоли надпочечников
Мало найдется заболеваний у человека, имеющих настолько разнообразную клиническую картину, как опухоль надпочечника. Симптомы этого заболевания могут быть связаны как со строением опухоли (доброкачественная или злокачественная), так и с наличие или отсутствием у опухоли гормональной активности.
Если симптомы злокачественности опухоли надпочечника достаточно типичны для всех злокачественных опухолей (похудание, появление болей, появление нарушений пищеварения, нарушений функции сосудов и т.д.), то гормональные симптомы таких опухолей зависят только от того, какой конкретно гормон вырабатывает опухоль (кортизол, альдостерон, половые гормоны, адреналин, норадреналин).
Гормональные симптомы опухоли надпочечника могут включать в себя появление ожирения, мышечной слабости, развитие остеопороза, депрессий, растяжений на коже (при кортизол-вырабатывающей опухоли коры надпочечника), кризового или постоянного повышения артериального давления (при феохромоцитоме – опухоли, вырабатывающей адреналин или норадреналин; при альдостероме – опухоли, вырабатывающей альдостерон), развития ряда мужских половых признаков (выраженной мускулатуры, оволосения, грубого голоса) при вирилизующей аденоме надпочечника (андростероме), вырабатывающей половые гормоны.
К счастью, злокачественные опухоли надпочечников (адренокортикальный рак, злокачественная феохромоцитома) встречаются достаточно редко – в 1-2% от всех опухолей. В большинстве случаев уже к моменту выявления эти опухоли имеют значительный размер (более 4 см) и часто сопровождаются регионарными метастазами (в лимфоузлы) или отдаленными метастазами (в легкие, кости). Злокачественные опухоли надпочечника требуют быстрого и радикального лечения.
Диагностика феохромоцитомы
Диагностика феохромоцитомы основывается на гормональных исследованиях и лучевых методах, позволяющих прямо визуализировать опухоль. Эти два направления отвечают каждое за свою часть обследования: гормональные исследования ставят своей целью обнаружение избыточной выработки катехоламинов, а лучевые методы призваны выявить или исключить наличие феохромоцитомы в надпочечнике или других областях.
Лабораторная диагностика феохромоцитомы в первую очередь основывается на использовании наиболее точного теста, которым является определение уровня метанефринов в суточной моче. В настоящее время четко показано, что определение уровня метанефринов является более точным, чем определение уровня самих катехоламинов (адреналина и норадреналина). Это связано с тем фактом, что часть феохромоцитом не выделяет адреналин и норадреналин прямо в кровь, а производит присоединение метильной группы к гормонам внутри своей ткани – при этом в кровь (и потом – в мочу) поступают уже конечные производные обмена – метанефрины. Определение уровня метанефринов в крови достаточно сложно, в связи с чем риск лабораторной ошибки при этом анализе достаточно высок. В суточной моче метанефрины накапливаются в течение долгого времени, их уровень там более стабилен, чем в крови – поэтому и метод этот применяется более часто.
Определение уровня катехоламинов (адреналина и норадреналина) в крови или суточной моче можно не проводить (в условиях, когда есть возможность выполнить исследование суточной мочи на метанефрины). Уровень катехоламинов в крови очень изменчив и зависит от массы внешних факторов, в связи с чем определение уровня адреналина и норадреналина способно привести к возникновению диагностической ошибке и либо установления ошибочного диагноза феохромоцитомы в условиях ее отсутствия, либо к пропуску имеющейся феохромоцитомы и возникновению связанных с этим осложнений и опасностей.
При обследовании пациента с подозрением на феохромоцитому производится и определение уровня хромогранина А, АКТГ, альдостерона, ренина, кальцитонина, кортизола крови. Хромогранин А является универсальным транспортным белком, вырабатываемым всеми видами нейроэндокринных опухолей, к которым относится и феохромоцитома. Его повышение в крови дает дополнительное подтверждение наличия феохромоцитомы надпочечника или параганглиомы (атипично расположенной феохромоцитомы).
Лучевая диагностика феохромоцитомы проводится с использованием компьютерной томографии с внутривенным введением контраста, накапливаемого некоторыми опухолями надпочечников. До, в процессе и после введения контраста проводится определение плотности образования надпочечника – на основании различий между нативной плотностью (т.е. плотностью образования до введения контраста в вену), плотностью в артериальную и венозную фазы (т.е. во время введения контраста) и отсроченной плотностью (т.е. плотностью после окончания введения контраста) врачи могут делать предположения о возможной природе опухоли. Злокачественные опухоли надпочечника обычно имеют высокую исходную плотность и активно накапливают контраст, после чего надолго задерживают его в своей ткани. Доброкачественные же опухоли, наоборот, характеризуются низкой нативной плотностью, активным накоплением контраста и последующим быстрым его вымыванием с возвращением плотности практически к исходным значениям.
В ряде случаев в качестве уточняющего метода диагностики может применяться сканирование с метайодбензилгуанидином (МИБГ) – изотопом, активно накапливающимся тканью таких опухолей, как феохромоцитома. Однако данное исследование не является основным, применяется далеко не у всех пациентов.
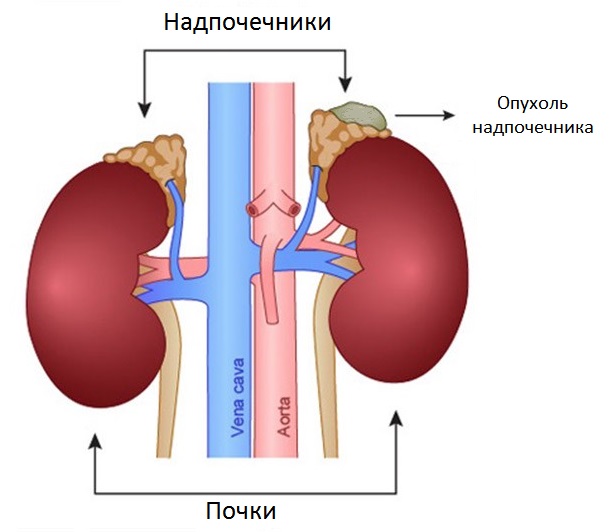
Анатомия и физиология надпочечников
- В мозговом слое вырабатываются биологически активные вещества: адреналин, норадреналин.
- В корковом слое синтезируются:
- Глюкокортикоиды (кортизол, кортикостерон)
- Минералокортикоиды – альдостерон
- Стероидные гормоны – мужские и женские половые гормоны (тестостерон и эстрогены соответственно).
- Глюкокортикоиды обладают очень важными свойствами и способствуют нормальному обмену веществ в организме. Влияют на обмен белков, жиров и углеводов. Поддерживают водно-солевой обмен в организме. Функция глюкокортикоидов не заканчивается на вышесказанном, и будет постепенно раскрываться по мере описания симптомов заболевания.
- Минералокортикоиды – поддерживают баланс таких минералов как натрий и калий. Увеличивают концентрацию натрия в организме, а вместе с ним и воду, таким образом, повышают артериальное давление крови.
- Стероидные гормоны – вырабатываются в небольших количествах и участвуют в созревании половых органов подростков, стимулируют появление вторичных половых признаков (специфическое оволосенение, рост молочных желез, и развитие скелета по мужскому или женскому типам), а также поддерживают сексуальную функцию, увеличивают половое влечение, и участвуют в поддержании нормального менструального цикла.
Методы диагностики заболеваний надпочечников
Для определения функционального состояния надпочечников используются методы лабораторной диагностики. Инструментальные методы используются для установления размеров надпочечников и выявления новообразований.
Анализ крови на гормоны
Анализ крови на гормоны является основным лабораторным методом диагностики заболеваний надпочечников. Имеют значение, прежде всего, такие показатели, как кортизол, альдостерон, ДГЭА-сульфат.
Суточный анализ мочи
Для оценки функции надпочечников применяется также суточный анализ мочи на кортизол.
Магнитно-резонансная томография (МРТ)
МРТ является одним из наиболее чувствительных методов инструментальной диагностики, используемых для выявления опухолей надпочечников.
Компьютерная томография (КТ)
Компьютерная томография (МСКТ почек и надпочечников) в настоящее время является наиболее распространённым методом диагностики новообразований надпочечников.
Другие методы инструментальной диагностики
УЗИ почек и надпочечников не является достаточно надёжным средством обнаружения новообразований надпочечников. Надпочечники на УЗИ не всегда удаётся визуализировать. Рентгенография (обычный рентген) для обследования надпочечников сегодня практически не применяется. Её место заняла компьютерная томография (как более информативный метод исследования). В отдельных случаях используется сцинтиграфия надпочечников.
Чтобы точно продиагностировать заболевание, запишитесь на прием к специалистам сети «Семейный доктор».
Надпочечниковая недостаточность — виды
Надпочечники — это небольшие железы, расположенные над почками, вырабатывая жизненно важные гормоны, в том числе кортизол. При надпочечниковой недостаточности надпочечники не вырабатывают достаточного количества определенных гормонов. Это приводит к снижению уровня кортизола, гормона стресса, который важен для многих функций организма. Существует три типа надпочечниковой недостаточности:
- Первичная надпочечниковая недостаточность, или болезнь Аддисона: повреждение надпочечников влияет на выработку гормонов.
- Вторичная надпочечниковая недостаточность: гипофиз головного мозга не вырабатывает достаточного количества адренокортикотропного гормона, который влияет на выработку кортизола в надпочечниках. Это приводит к снижению уровня гормонов.
- Третичная надпочечниковая недостаточностьгипоталамус в головном мозгу, область, которая влияет на выработку гормонов в надпочечниках, производит слишком мало кортикотропин-рилизинг-гормона, что снижает уровень гормонов.
Гормоны надпочечников влияют на многие функции организма. Примеры данных гормонов включают кортизол, который помогает контролировать артериальное давление, воспаление и обмен веществ, в то время как альдостерон уравновешивает минералы в крови. Надпочечниковая недостаточность вызывает широкий спектр симптомов, от слабости до снижения уровня сахара в крови.
Этиология и классификация
Недостаточность надпочечниковых желез может быть острой (гипоадреналовый криз) — резкое разрушение коры надпочечников при двустороннем кровоизлиянии в надпочечники (Синдром Уотерхауса-Фридериксена), повреждение надпочечников в результате травмы или хирургического вмешательства и хронической (аутоиммунный процесс, туберкулёз и другие).
Острая надпочечниковая недостаточность
Острая недостаточность коры надпочечников характеризуется крайне низкой концентрацией в плазме крови кортизола, кортикостерона, альдостерона, дезоксикортикостерона. Экскреция 17-оксикортикостероидов также заметно снижена. Содержание в плазме крови АКТГ высокое. Имеются признаки нарушения минерального и водного обмена.
Хроническая надпочечниковая недостаточность
Хроническая недостаточность коры надпочечников — в 85 % случаев представляет собой аутоиммунное поражение надпочечников, а также результат деструкции надпочечников при
- инфаркте надпочечников,
- туберкулёзе,
- саркоидозе,
- амилоидозе,
- послеоперационных осложнениях,
- злокачественных новообразованиях,
- поражении надпочечников фармакологическими препаратами (антикоагулянты, этомидат, блокаторы стероидогенеза, хлодитан, барбитураты, спиронолактон, кетоконазол и другие),
- гемохроматозе,
- полигландулярном эндокринном синдроме,
- адренолейкодистрофии (англ.)русск.,
- адреномиелодистрофии,
- гипоплазии,
- дефекте ферментов синтеза гормонов коры надпочечников,
- последствия радиотерапии,
- идиопатические случаи.
Кроме того, различают:
Первичный гипокортицизм
Перви́чная надпо́чечниковая недоста́точность — результат непосредственного поражения надпочечников, вследствие которого разрушается более 90 % клеток коркового вещества, секретирующих кортикостероиды.
Вторичный гипокортицизм
Втори́чная надпо́чечниковая недоста́точность обусловлена патологией гипофиза, приводящей к дефициту секреции кортикотропина (АКТГ). Вторичный гипокортицизм обычно сочетается с недостаточностью других эндокринных же́лез и дефицитом гормона роста (СТГ).
Третичный гипокортицизм
Трети́чная надпо́чечниковая недоста́точность развивается при различных поражениях гипоталамической области, чаще опухолевого или воспалительного характера. Заболевание развивается после 30 лет, женщины болеют вдвое чаще мужчин. Распространённость около 4-11 случаев на 100 тысяч населения.
Ятрогенный гипокортицизм
Ятрогенная надпочечниковая недостаточность (27.3 по МКБ-10) развивается после прекращения терапии глюкокортикоидами в результате быстрого падения уровня эндогенных глюкокортикоидных гормонов на фоне длительного угнетения синтеза АКТГ экзогенными глюкокортикоидами. У разных пациентов устойчивость эндокринной системы к действию экзогенных глюкокортикоидов неодинакова.
Клиническая картина
Представлена типичными симптомами угнетения гипоталамо-гипофизарно-надпочечниковой системы после отмены терапии глюкокортикоидами:
- слабость
- утомляемость
- депрессия
- артериальная гипотония
- обострение основного заболевания, по поводу которого была назначена терапия глюкокортикоидами
На фоне тяжёлого стресса, если пациенту вовремя не увеличена доза глюкокортикоидов, может развиться гипоадреналовый криз.
Клинические симптомы могут отсутствовать и только биохимические нарушения (снижение секреции кортизола в пробах с АКТГ) свидетельствуют о недостаточности гипоталамо-гипофизарно-надпочечниковой системы. В таких случаях заболевание проявляется резкой слабостью во время или после незначительных стрессов или недомоганий, например при респираторных инфекциях.
Диагностика
Ятрогенную надпочечниковую недостаточность следует заподозрить:
- у любого пациента, получавшего преднизолон в дозе 15—30 мг/сут на протяжении 3—4 недель. В этом случае угнетение гипоталамо-гипофизарно-надпочечниковой системы после отмены терапии глюкокортикоидами может сохраняться в течение 8—12 месяцев.
- у любого пациента, получавшего преднизолон в дозе 12,5 мг/сут а протяжении 4 недель. При этом угнетение гипоталамо-гипофизарно-надпочечниковой системы после отмены терапии глюкокортикоидами может сохраняться в течение 1—4 месяцев.
- у любого пациента с синдромом Кушинга после удаления аденомы или злокачественного новообразования надпочечника.
- у любого пациента со снижением секреции кортизола в ответ на введение АКТГ, если он получает глюкокортикоиды (независимо от дозы и продолжительности глюкокортикоидной терапии).
Профилактика
Применение терапии глюкокортикоидами в объёмах и продолжительности в соответствии с современными рекомендациями, поэтапная отмена терапии.
Причины и механизмы развития хронической надпочечниковой недостаточности
Основной причиной первичного гипокортицизма считают аутоиммунное поражение коры надпочечников, так как оно встречается у половины больных, и может сочетаться с рядом других аутоиммунных эндокринных патологий типа сахарного диабета, гипопаратиреоза, аутоиммунного тиреоидита, витилиго и пр., приводя к развитию полиэндокринного синдрома (аутоиммунного полигландулярного синдрома – одновременному поражению нескольких эндокринных желез со снижением их функции).
Другой причиной поражения коры надпочечников считается заражение туберкулезом, причем у взрослых эта причина более распространенна, чем у детей, и процесс обычно сочетается с туберкулезом легких. Кроме того, причинами, вызывающими хроническую надпочечниковую недостаточность, являются метастазы в надпочечники опухолей, расположенных в других органах, инфекционные поражения надпочечников вирусами, бактериями, грибками, хирургическое вмешательство или полное удаление надпочечников, кровоизлияние
в ткани надпочечников из-за применения антикоагулянтов.
Вторичный и третичный гипокортицизм развиваются на фоне деструктивных, травматических или опухолевых процессов в гипофизе и гипоталамусе, результатом которых становится нарушение кортикотропной функции (выработки АКТГ – адренокортикотропного гормона). Заболевания сосудов и гранулематозные процессы данной области, вызванные инфекционными агентами, также способствуют развитию хронической надпочечниковой недостаточности.
При первичном гипокортицизме из-за снижения продукции гормонов коры надпочечников — кортизола и альдостерона, нарушается водно-солевой метаболизм и другие обменные процессы в организме. Прогрессирующее обезвоживание, возникающее из-за снижения секреции альдостерона, неблагоприятно сказывается на деятельности пищеварительной и сердечно-сосудистой систем (снижается артериальное давление). Помимо этого, дефицит кортизола приводит к развитию гипогликемии, вызывающей мышечную слабость, а также к стимуляции выработки адренокортикотропного и меланоцитостимулирующего гормона гипофизом, в результате чего у больных развивается гиперпигментация кожных покровов и слизистых оболочек. Специфический цвет кожи больных объясняет одно из названий первичного гипокортицизма — бронзовая болезнь. Недостаточный уровень андрогенов, секретируемых надпочечниками, приводит к задержке роста и полового созревания.
При вторичной хронической почечной недостаточности наблюдается недостаток кортизола, а секреция альдостерона сохраняется в норме. В связи с этим вторичная хроническая надпочечниковая недостаточность протекает легче первичной.