Свистящее дыхание
Содержание:
- К каким докторам обращаться, если у Вас фиброз легких
- Как лечить фиброз легких?
- Лечение фиброза легких во время беременности
- 1.Общие сведения
- Лечение эмфиземы легких
- Виды легочного фиброза
- Злокачественные новообразования легкого
- С какими заболеваниями может быть связано
- Хирургическое лечение
- Альфа-фетопротеин
- Обострение ИЛФ
- Используемые источники
- Диагностика
- 2.Причины
- Лечение фиброза легких во время беременности
- Консервативное лечение
- Как лечить фиброз легких?
- Онкология
- Лечение радиоактивным йодом
- Биопсия легкого
К каким докторам обращаться, если у Вас фиброз легких
Диагностика фиброза легких основывается на анализе клинических критериев:
- прогрессирующая одышка,
- кашель,
- общая слабость,
- снижение массы тела.
Целесообразно провести анамнез жизни пациента для получения информации о перенесенных и имеющихся заболеваниях:
- пневмония,
- туберкулез (инфекционное заболевание, вызываемое микобактерией туберкулеза),
- системная склеродермия,
- ревматоидный артрит,
- вредная профессиональная деятельность, например, на производстве.
Специфическая диагностика представлена следующими процедурами:
- аускультация (выслушивания) и перкуссия (простукивания) легких;
- спирография (исследование объема легких и дыхательной функции);
- рентгенография грудной клетки (позволяет обнаружить изменения в легких);
- компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) — позволяют наиболее детально определить характер изменений в легких;
- биопсия легкого — исследование кусочка ткани легкого, полученного при эндоскопическом исследовании бронхов (введение в дыхательные пути бронхоскопа) или во время операции; позволяет обнаружить рубцовую ткань в легком на микроскопическом уровне.
Как лечить фиброз легких?
Лечение фиброза легких определяется квалифицированным специалистом в зависимости от особенностей течения заболевания у конкретного человека. К тяжелым формам фиброза применяются глюкокортикоиды, цитостатики и иммунодепрессанты. Пораженные фиброзом легкие часто становятся благоприятной средой для присоединения патогенной микрофлоры и развития воспаления. Чтобы воспрепятствовать этому, назначаются антибактериальные препараты, полезными будут кислородные ингаляции и сердечные гликозиды. При изнуряющем кашле и одышке назначаются бронхорасширяющие препараты.
Медикаментозное лечение фиброза легких должно быть подкреплено лечебной дыхательной гимнастикой, в то время как крупные физические нагрузки больному противопоказаны. Также необходимо исключить воздействие на организм провоцирующих фиброз факторов.
Специфической терапии фиброза не разработано, патологический процесс такого рода до сих пор считается необратимым. Перед врачом стоит задача не допустить его прогрессирования, присоединения вторичной инфекции и максимально улучшить качество жизни пациента. Для достижения этих целей применяются такие терапевтические методики:
- кислородотерапия — ингаляции кислорода с помощью специальных аппаратов;
- дыхательная гимнастика;
- оперативное вмешательство — допустимо при тотальном фиброзе, представлено трансплантационными методиками.
Лечение фиброза легких во время беременности
Лечение фиброза легких необходимо проходить под наблюдением компетентного специалиста, который оценит пользу лечения для матери и риск от такой терапии для плода. Лечебные назначения осуществляются в зависимости от степени фиброза и особенностей его течения. Если заболевание серьезным образом не отражается на здоровье женщины и не грозит осложниться в течение беременности или родов, можно отложить лечение на послеродовой период. Однако наличие такого диагноза определяет необходимость находиться под медицинским контролем, чтобы вовремя среагировать ухудшение самочувствия.
1.Общие сведения
Слово «метастаз» в общественном сознании давно ассоциируется с «той самой болезнью» и воспринимается как неумолимый приговор. Учитывая перевод с латыни, этот термин означает перемещение, перенос патологического процесса из первичного очага – с развитием вторичных очагов в иных органах. Строго говоря, в медицине метастазами называют не только онкологическую экспансию, но и инфекционную, и все же почти всегда под метастазированием подразумевается именно злокачественный процесс в его отдаленных стадиях. Однако абсолютным приговором метастатический рак больше не является, и это, пожалуй, главная информация в данной статье.
Рак легкого как первичный очаг встречается значительно реже, чем метастазы в легких, и этот первичный вариант в прогнозе дальнейшего распространения является неблагоприятным: из легочных тканей незрелые раковые клетки разносятся быстро, и практически всегда (80-100% наблюдений) метастазируют в позвоночнике, печени, костных тканях, головном мозгу и т.д. Как место локализации вторичных опухолей легкие также относятся к наиболее вероятным мишеням (статистические оценки частоты варьируют между первым и вторым местами). При онкологическом обследовании метастазы ищут прежде всего в грудной клетке – и нередко находят, причем в большинстве случаев легкие оказываются единственным, изолированным очагом вторичного поражения.
Лечение эмфиземы легких
Мер специфического лечения данного заболевания на сегодня не существуют. Актуальны терапевтические программы, как и при всех ХОБЛ. Нужно устранить факторы, которые вызвали развитие эмфиземы. Это может быть инфекционный процесс хронического характера в дыхательных путях, действие грязного воздуха, курение и пр.
Медикаментозное лечение включает прием средств для расширения бронхов:
- сальбутамол или фенотерол
- М-холиноблокаторы
- формотерол или салметерол
- комбинация выше названных препаратов
- препараты теофиллина пролонгированного действия
Людям в возрасте лучше назначать м-холиноблокаторы. Теофиллины для них почти никогда не актуальны.
Глюкокортикоиды эффективны при тяжелом течении эмфиземы легких. Назначается преднизолон короткими курсами преднизолона до 20-30 мг внутрь с быстрым снижением дозы и отменой препарата на протяжении 7-12 дней. Необходим контроль эффективности терапии по кривой «поток-объем». Если эффекта не достигают, то ГК больше давать пациенту не нужно. При положительном действии системных ГК лучше всего продолжать применять ингаляционные лекарства. Например, эффективен будесонидом по 400-500 мкг 2 раза в сутки.
Заместительная терапия человеческим альфа-1-антитрипсином может дать нужный эффект, особенно при генетической предрасположенности к рассматриваемому заболеванию. Но в клиническую практику на сегодня не внедрен ни один из препаратов этого ряда.
Ацетилцистеин оказывает антиоксидантное действие. Внутрь назначают по 600 мг, прием 1 раз в сутки перед сном.
Хирургическое лечение заключается в уменьшении объема легких. Проводится буллэктомия, лучше всего — торакоскопическая. Делают резекцию периферических участков легких, потому остальные участки декомпрессируются. Функциональное состояние легких улучшается. Медики также пытаются внедрить метод трансплантации легких, в том числе в странах СНГ. При развитии спонтанного пневмоторакса применяют дренирование плевральной полости и аспирация воздуха.
Виды легочного фиброза
Существует более 200 видов легочного фиброза, и наиболее распространенным из них является ИЛФ. Существует пять основных категорий легочного фиброза, основанных на их причинах:
- Лекарственно-индуцированный: причиной является применение препаратов, влияющих на легкие, таких как химиотерапия, Амиодарон (Пейсерон) или Нитрофурантоин (Макробид).
- Радиационно-индуцированный: вследствие лучевой терапии грудной клетки.
- Легочный фиброз окружающей среды: из-за воздействия раздражителей легких, таких как плесень.
- Аутоиммунный: вследствие аутоиммунных заболеваний, таких как ревматоидный артрит или синдром Шегрена.
- Профессиональный: вследствие воздействия пыли или паров, таких как асбест или кремнезем.
ИЛФ отличается от других форм легочного фиброза тем, что у него нет известной причины.
Злокачественные новообразования легкого
Опыт хирургического лечения рака легкого – это более 5 тысяч операций, использование – совместно с профильными отделениями НМИЦ онкологии им. Н.Н.Блохина – пред- и послеоперационной лекарственной и лучевой терапии, множество научных публикаций, выступлений на международных и российских съездах и конференциях. Основным подходом в хирургии рака легкого является выполнение радикальной операции в объеме пневмонэктомии или лобэктомии с систематической медиастинальной ипсилатеральной лимфодиссекцией (полноценное, выполняемое всегда, удаление клетчатки с лимфатическими узлами переднего, заднего, верхнего и нижнего средостения на стороне поражения независимо от локализации опухоли в легком и размеров лимфатических узлов), позволяющей повысить радикальность хирургического вмешательства, а также объективизирующей распространенность опухолевого процесса. В силу необходимости соблюдения радикализма эти операции дополняются резекцией соседних органов при их поражении (грудной стенки, диафрагмы, крупных сосудов – верхней полой вены, легочной артерии, аорты и ее ветвей, предсердия, перикарда, бифуркации трахеи, пищевода и т.д.).
Торакальное отделение обладает на сегодняшний день одним из наиболее крупных в мире, и самым большим в России опытом выполнения полностью торакоскопических лобэктомий с медиастинальной лимфодиссекцией при немелкоклеточном раке легкого. Подобная операция (когда оперативное вмешательство выполняется исключительно из так называемых точек доступа – торакопортов, а миниторакотомия производится в конце оперативного вмешательства для эвакуации удаленного препарата), в России впервые была выполнена в торакальном отделении Онкологического центра в 2007 году. На сегодняшний день с применением торакоскопической методики прооперировано более 400 пациентов первичным раком легкого. Продолжительность нахождения пациентов в стационаре после торакоскопической лобэктомии в среднем составляет 5 суток, снижается до минимума послеоперационный болевой синдром и частота послеоперационных осложнений.
Торакоскопический доступ широко используется при метастатическом поражении легких и лимфоузлов средостения. Зачастую у онкобольных появляются новые метастазы в легких и требуют повторного удаления, торакоскопический доступ, в отличии от торакотомии, позволяет избегать образования спаек в плевральной полости, и выполнить повторную операцию с наименьшей травматичностью.
Опухоли трахеи
Основным методом лечения злокачественных опухолей трахеи является хирургический. При раннем раке трахеи рекомендуется рассматривать возможность применения органосохранных и функционально-щадящих способов лечения, таких как эндоскопическая резекция слизистой с подслизистой диссекцией, с высокой эффективностью.
На боле поздних стадиях выполняется циркулярная резекция трахеи с формированием одномоментного межтрахеального анастамоза, а при поражении бифуркации трахеи, и с формированием искусственной карины, и обязательным выполнением паратрахеальной и бифуркационной медиастинальной лимфодиссекции.
Опухоли вилочковой железы
Тимомы являются наиболее частыми опухолями средостения. Основной метод лечения – оперативное удаление. При неинвазивном росте и небольших размерах опухоли выполняется торакоскопическая тимтимомэктомия, при больших размерах и врастании в соседние анатомические структуры применяется открытый доступ – стернотомия.
С какими заболеваниями может быть связано
Патологический процесс в легких, с течением времени ведущий к замещению нормальной ткани соединительной, оказывается смежным или последующим со следующими состояниями:
- альвеолит — патологический процесс в интерстициальной ткани легких, часто оказывающийся предшественником прогрессирующего фиброза; проявляется обычно нарастающей дыхательной недостаточностью;
- асбестоз — патологическое состояние, относящееся к группе пневмокониозов, развивающееся вследствие длительного контакта с асбестовой пылью;
- гранулематоз легкого;
- микозы легких — грибковые поражения легочной ткани, возникающие преимущественно у пациентов с резко сниженными защитными реакциями организма
- пневмокониоз — заболевания легких, которые развиваются в результате вдыхания человеком пыли;
- сахарный диабет;
- силикоз — патологическое состояние, относящееся к группе пневмокониозов, развивающееся вследствие длительного контакта с частицами пыли, содержащей силикаты;
- травмы легкого;
- туберкулез легких — инфекционное заболевание, вызываемое несколькими разновидностями кислотоустойчивых микобактерий, максимально часто опражающих именно легкие.
Осложнениями фиброза легких при неадекватном или несвоевремнном лечении становятся:
- хроническая дыхательная недостаточность;
- легочная гипертензия;
- хроническое легочное сердце;
- присоединение вторичной инфекции (с развитием пневмонии).
Хирургическое лечение
Радикальный метод, который заключается в полном удалении ткани щитовидной железы (обеих долей и перешейка). Операция сложная, требуется сохранить все органы, расположенные рядом, в том числе возвратный нерв и паращитовидные железы. В некоторых случаях удаление выполняется из традиционного открытого доступа, в других – используется эндоскопическая техника. Все зависит от особенностей случая и тяжести тиреотоксикоза.
Показания к операции:
- аллергия на тиреостатики;
- лейкопения (уменьшение количества лейкоцитов) на фоне приема тиреостатиков;
- зоб третьей и последующих стадий;
- разрастание железы на фоне медикаментозного лечения (зобогенный эффект);
- тяжелые сердечно-сосудистые нарушения.
Альфа-фетопротеин
Альфа-фетопротеин (АФП) эффективен при лечении заболеваний с аутоиммунной компонентой и ряда других трудноизлечимых и ранее неизлечимых заболеваний:
* поражение легких различной степени тяжести;
— не специфические язвенные колиты (НЯК), болезнь Крона, поражения щитовидной железы (аутоиммунный тиреоидит, Хашимото и др), хронические окклюзионне заболевания сосудов (тромбангииты, облитерирующие эндартерииты, атеросклероз и инфекционно — аллергические артерииты) ревматоидные артриты, рассеянный склероз, миастения Грэвиса, поражения поджелудочной железы, диабет и др.
— заболевания печени различной этиологии: аутоиммунные, вирусные гепатиты (ВГ), циррозы;
— заболевания сердца, вызванные поражениями сосудов (предынфарктное состояние, инфарктное состояние, постинфарктное состояние, другие нарушения коронарного кровообращения, постинфекционные осложнения, реабилитация после шунтирования сосудов сердца и т.д.);
— гиперпластические патологии в гинекологии: миомы, фибромы и фиброзы матки, состояние после лечения непроходимости труб, кисты яичника, а также мастопатия, в том числе тяжелые формы, предраковые состояния;
— тяжелые ожоги и ожоговая болезнь, пересадки кожи;
Обострение ИЛФ
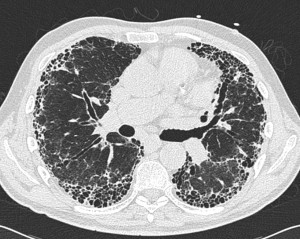
Обострение ИЛФ – это тяжелое жизнеугрожающее состояние, проявляющееся в виде быстрого нарастания дыхательной недостаточности у пациентов с ранее установленным диагнозом ИЛФ . Как правило, характеризуется крайне тяжелым течением; смертность в ряде исследований достигала 85% . В отличие от стабильного или медленно прогрессирующего течения ИЛФ, критерии диагностики его обострения определены менее четко. Согласно данным Н. Collard и соавт. , критерии обострения ИЛФ включают в себя наличие предшествующего или впервые выявленного ИЛФ с резким нарастанием одышки, развитием дыхательной недостаточности за предшествующие 30 дней без установленной причины, а также появление новых зон затемнения легочной ткани по типу «матового стекла» и/или консолидации на фоне имевшихся ранее изменений, соответствующих ОИП – зон ретикулярных изменений и «сотового легкого» (рис. 4) . Тем не менее, вышеуказанные критерии обладают низкой специфичностью, в связи с чем при подозрении на обострение ИЛФ должен проводиться дифференциальный диагноз с инфекционным процессом, тромбоэмболией легочной артерии и ее ветвей, пневмотораксом, а также острой левожелудочковой недостаточностью с развитием отека легких .
Используемые источники
- Raghu G, Anstrom KJ, King TE Jr, et al. Prednisone, azathioprine, and N-acetyl-cysteine for pulmonary fibrosis. N Engl J Med 2012;366(21):1968-77.
- Richeldi L, du Bois RM, Raghu G, et al. Efficacy and safety of nintedanib in idio-pathic pulmonary fibrosis. N Engl J Med 2014;370(22):2071-82. .
- Noble PW, Albera C, Bradford WZ, et al. Pirfenidone for idiopathic pulmonaryfibrosis: analysis of pooled data from three multinational phase 3 trials. Eur RespirJ 2016;47(1):243-53.
- Collins BF, Raghu G. Antifibrotic therapy for fibrotic lung disease beyond idio-pathic pulmonary fibrosis. Eur Respir Rev 2019;28(153).
- Wollin L, Distler JHW, Redente EF, et al. Potential of nintedanib in treatment ofprogressive fibrosing interstitial lung diseases. Eur Respir J 2019;54(3).
- Distler O, Highland KB, Gahlemann M, et al. SENSCIS Trial Investigators.Nintedanib for systemic sclerosis-associated interstitial lung disease. N Engl J Med2019;380(26):2518-28.
- Hudson M, Thombs B, Baron M, et al. Time to diagnosis in systemic sclerosis: issex a factor? Arthritis Rheum 2009;61(2):274-8.
- Ананьева Л.П. Новые классификационные критерии системной склеродер-мии. Научно-практическая ревматология 2013;51(5):539-44 .
- Tyndall AJ, Bannert B, Vonk M, et al. Causes and risk factors for death in sys-temic sclerosis: a study from the EULAR Scleroderma Trials and Research(EUSTAR) database. Ann Rheum Dis 2010;69(10):1809-15.
- Bussone G, Mouthon L. Interstitial lung disease in systemic sclerosis. AutoimmunRev 2011;10(5):248-55.
- Теплова Л.В., Ананьева Л.П., Лесняк В.Н. и др. Системная склеродермия синтерстициальным поражением легких: сравнительная клиническая харак-теристика с больными без поражения легких. Научно-практическая ревма-тология 2010;3:36-41 .
- Чотчаева Ф.Р., Зыкова А.С., Новиков П.И., Моисеев С.В. Диагностика илечение системной склеродермии. Клин фармакол тер 2018;27(1):66-73.
- Hoyles RK, Ellis RW, Wellsbury J, et al. A multicenter, prospective, random-ized,double-blind, placebo-controlled trial of corticosteroids and intra-venous cyclophosphamide followed by oral azathioprine for the treatment ofpulmonary fibrosis in scleroderma. Arthritis Rheum 2006;54(12):3962-70.
- Tashkin DP, Elashoff R, Clements PJ, et al. Effects of 1-year treatment withcyclophosphamide on outcomes at 2 years in scleroderma lung disease. Am JRespir Crit Care Med 2007;176(10):1026-34.
- Tashkin DP, Roth MD, Clements PJ, et al. Mycophenolate mofetil versus oralcy-clophosphamide in scleroderma-related interstitial lung disease (SLS II):a ran-domised controlled, double-blind, parallel group trial. LancetRespir Med 2016;4(9):708-19.
- Ананьева Л.П., Десинова О.В., Конева О.А. и др. Лечение ритуксимабоминтерстициального поражения легких при системной склеродермии.Научно-практическая ревматология 2013;51(5):514-23 .
- Elhai M, Boubaya M, Distler O, et al. Outcomes of patients with systemic sclero-sis treated with rituximab in contemporary practice: a prospective cohort study.Ann Rheum Dis 2019;78(7):979-87.
- Oldham JM, Adegunsoye A, Valenzi E, et al. Characterisation of patients withinterstitial pneumonia with autoimmune features. Eur Respir J 2016;47(6):1767-75.
Диагностика
ЭКГ. Инструментальные исследования дают возможность выявить нарушения функции внешнего дыхания, характерно значительное уменьшение ЖЕЛ. На электрокардиограмме у таких больных часто наблюдаются экстрасистолы, признаки замедления внутрижелудочковой проводимости и нарушения коронарного кровообращения.
Рентген. Рентгенологическое исследование является решающим в диагностике релаксации, при этом определяются следующие симптомы:
- стойкое повышение уровня расположения соответствующего купола диафрагмы до 2 – 5 ребра;
- в горизонтальном положении диафрагма и прилежащие к ней органы брюшной полости смещаются кверху;
- контур диафрагмы представляет собой ровную, непрерывную дугообразную линию.
Нередко выявляется ателектаз нижних отделов легкого и смещение средостения.
Релаксация диафрагмы рентген (левый купол)
КТ. Наиболее информативным методом исследования является компьютерная томография, дающая полную информацию о степени релаксации и характере изменений органов грудной и брюшной полостей. Во всех случаях релаксации, даже при небольшой ее выраженности, наблюдается ателектаз и воспалительные изменения базальных сегментов легкого. С внедрением компьютерной томографии практически отпала надобность в остальных традиционных методах дифференциальной диагностики.
Релаксация правого купола диафрагмы на КТ
2.Причины
Предназначение и, соответственно, строение газообменной биосистемы, – которой и являются легкие, – требует высокой концентрации кровеносных и лимфатических сосудов. Циркуляция крови и лимфы в легких очень интенсивна и разветвлена, здесь много лимфатических узлов, рядом пищевод, крупная аортально-венозная сеть, сердце с системой коронарных артерий. Учитывая, что двумя основными путями миграции раковых клеток в организме являются гематогенный (с током крови) и лимфагенный (по лимфатическим протокам), легкие представляют собой ближайший и практически идеальный плацдарм для развития вторичных опухолевых процессов.
Лечение фиброза легких во время беременности
Лечение фиброза легких необходимо проходить под наблюдением компетентного специалиста, который оценит пользу лечения для матери и риск от такой терапии для плода. Лечебные назначения осуществляются в зависимости от степени фиброза и особенностей его течения. Если заболевание серьезным образом не отражается на здоровье женщины и не грозит осложниться в течение беременности или родов, можно отложить лечение на послеродовой период. Однако наличие такого диагноза определяет необходимость находиться под медицинским контролем, чтобы вовремя среагировать ухудшение самочувствия.
Консервативное лечение
Консервативное лечение заключается в постоянном приеме тиреостатических лекарств:
- тиамазол (тирозол, метизол, мерказолил);
- пропилтиоурацил (пропицил).
Действие этих лекарств основано на блокировании фермента пероксидазы, без которого невозможен полноценный синтез тиреоидных гормонов. Лекарства разрушают излишки гормонов, циркулирующих в крови, и постепенно накапливаются в железе. Поэтому эти лекарства нужно принимать пожизненно, так как при их отмене концентрация тиреоидных гормонов возрастает очень быстро.
Первоначально лекарства принимаются в высоких дозах, так делают до нормализации уровня гормонов. В дальнейшем переходят на поддерживающие дозы, периодически осуществляя лабораторный контроль.
Лечением беременных занимаются совместно и . Чаще всего используется пропицил, так как лекарство практически не проникает через плаценту. Используются по возможности минимальные дозировки. Растущий плод нейтрализует избыток тиреоидных гормонов, и с 25-й недели прием тиростатиков не требуется, как правило. До родов без лекарств можно обойтись. После родов происходит постепенное нарастание концентрации, и через 3 месяца прием лекарств приходится возобновлять.
Как лечить фиброз легких?
Лечение фиброза легких определяется квалифицированным специалистом в зависимости от особенностей течения заболевания у конкретного человека. К тяжелым формам фиброза применяются глюкокортикоиды, цитостатики и иммунодепрессанты. Пораженные фиброзом легкие часто становятся благоприятной средой для присоединения патогенной микрофлоры и развития воспаления. Чтобы воспрепятствовать этому, назначаются антибактериальные препараты, полезными будут кислородные ингаляции и сердечные гликозиды. При изнуряющем кашле и одышке назначаются бронхорасширяющие препараты.
Медикаментозное лечение фиброза легких должно быть подкреплено лечебной дыхательной гимнастикой, в то время как крупные физические нагрузки больному противопоказаны. Также необходимо исключить воздействие на организм провоцирующих фиброз факторов.
Специфической терапии фиброза не разработано, патологический процесс такого рода до сих пор считается необратимым. Перед врачом стоит задача не допустить его прогрессирования, присоединения вторичной инфекции и максимально улучшить качество жизни пациента. Для достижения этих целей применяются такие терапевтические методики:
- кислородотерапия — ингаляции кислорода с помощью специальных аппаратов;
- дыхательная гимнастика;
- оперативное вмешательство — допустимо при тотальном фиброзе, представлено трансплантационными методиками.
Онкология
При одновременном применении «Альфа-фетопротеин» повышает клиническую эффективность цитостатических препаратов при проведении системной химиотерапии у больных злокачественными опухолевыми заболеваниями, снижает токсический эффект цитостатиков за счет уменьшения цитолиза гепатоцитов и нефропротекторного действия. Повышает клиническую эффективность противовирусных препаратов (интерфероны).
Изобретение относится к области медицины, в частности к онкологии и может быть использовано для химиотерапевтического лечения онкологических больных, страдающих разными видами злокачественных новообразований.
Заявляемый способ заключается в введении больному нового комплексного препарата, обладающего противоопухолевой активностью, состоящего из векторной, специфической к раковым клеткам части (АФП) и не специфической части, содержащей цитотоксическое средство ( разрушающая ).
Известно использование АФП в качестве вектора для адресной доставки в раковую клетку цитотоксических препаратов (см. , например, Патент РФ 2071351, кл. А 61 К 38/17, опубл. 10.01.97). Во всех известных случаях АФП связан с цитотоксической частью препарата ковалентной химической связью, а в заявляемом комплексном препарате АФП с ПАВ образуют не ковалентный комплекс, одновременно обеспечивающий стабильность макромолекулы в процессе транспорта и функциональную независимость в процессе цитотоксического действия. Действие заявляемого комплексного препарата основано на инициации физиологической редукции раковых клеток по механизму, сходному с процессом апоптоза ( разрушения клетки ). Естественное саморазрушение клеток опухоли под действием препарата, как правило, не приводит к интоксикации организма, эффект лечения проявляется быстро.
Лечение радиоактивным йодом
Относится к эффективным и щадящим методам лечения, позволяет разрушить щитовидную железу без операции. Пациент принимает внутрь изотопы радиоактивного йода, который накапливается в железе. Там йод распадается, что вызывает местную гибель клеток.
Лечение требует ежедневного врачебного наблюдения, поэтому применяется только в стационарных условиях.
Часто радийодтерапия применяется вслед за операцией, чтобы подавить остатки гормоноактивной ткани железы. Комбинированное лечение дает абсолютно надежный результат, человек полностью освобождается от болезни.
- Узловой зоб
- Несахарный диабет
Биопсия легкого
Если однозначные данные о наличии ИЛФ при КТВР отсутствуют, то для подтверждения диагноза показано выполнение хирургической биопсии легких, которую чаще проводят с помощью видеоторакоскопической методики. С целью повышение эффективности биопсия легких должна производиться из разных долей легких. Хотя ХБЛ является наиболее достоверным методом определения гистологической картины ИИП, ее проведение связано с риском возникновения ряда осложнений, наиболее тяжелым из которых является обострение ИЛФ, особенно у пациентов с тяжелой дыхательной и/или сердечной недостаточностью . В связи с этим решение о ее проведении должно приниматься индивидуально с учетом клинической картины, возможных преимуществ для постановки точного диагноза, а также согласия пациента.
В течение последнего десятилетия для гистологического подтверждения диагноза ИЛФ и других вариантов ИИП разработана методика трансбронхиальной криобиопсии легкого (ТБКБЛ). Ее основными преимуществами являются малоинвазивность, отсутствие необходимости в проведении интубации и ингаляционного наркоза и, вследствие этого, низкая частота развития осложнений в сочетании с возможностью получения большого по объему биоптата легкого, достаточного, в абсолютном большинстве случаев, для гистологической верификации диагноза . Так, у пациентов без типичной картины ОИП по данным КТВР проведение ТБКБЛ позволяло установить диагноз приблизительно в 2/3 случаев, что сопоставимо с эффективностью ХБЛ в сходной ситуации . При этом для ТБКБЛ характерны более низкий риск периоперационных осложнений (чаще всего отмечают развитие пневмоторакса и не угрожающего жизни кровотечения в месте проведения биопсии) и смерти, более короткий период госпитализации, что позволяет проводить ТБКБЛ у пациентов с высоким уровнем анестезиологического риска и наличием противопоказаний к ХБЛ .Таким образом, внедрение ТБКБЛ в клиническую практику может расширить показания к биопсии легкого и повысить диагностическую точность алгоритма обследования пациентов с подозрением на ИЛФ.