Хромосомные аберрации в опухоли
Содержание:
Физико-химическая природа хромосом
Физико-химическая природа хромосом зависит от сложности организации биологического вида. Хромосома эукариот состоит из молекулы дезоксирибонуклеиновой кислоты (см.), гистоновых и негистоновых белков (см. Гистоны), а также рибонуклеиновой кислоты (см.). Основным химическим компонентом хромосомы, заключающим в структуре своей молекулы генетическую информацию, является ДНК. В естественных условиях в отдельных участках хромосомы ДНК может быть свободной от структурных белков, однако в основном она существует в виде комплекса с гистонами, причем как и в интерфазе, так и в метафазе весовое отношение ДНК/гистон составляет единицу. Содержание кислых белков в хромосомах варьирует в зависимости от их активности и степени конденсации в клеточном цикле. В хроматине (см.) интерфазного ядра и на любой стадии митотической конденсации ДНК существует в комплексе с гистонами, и взаимодействие именно этих молекул создает элементарные структурные частицы хроматина — нуклеосомы. В нуклеосоме ее центральную часть составляют 8 молекул гистонов четырех типов (по 2 молекулы от каждого типа). Это гистоны Н2А, Н2В, НЗ и Н4, взаимодействующие между собой, по-видимому, С-концевыми участками молекул. N-концевые участки гистоновых молекул взаимодействуют с молекулой ДНК таким образом, что последняя оказывается накрученной на гистоновый остов, делая два витка на одной его стороне и один на другой. На одну нуклеосому приходится около 140 пар оснований ДНК. Между соседними нуклеосомами имеется варьирующий по длине отрезок ДНК (10—70 пар оснований). Когда он выпрямлен, ДНК принимает вид нити с бусинками. Если отрезок находится в сложенном состоянии, нуклеосомы тесно прилегают друг к другу, формируя фибриллу диаметром 10 нм. Строение из нуклеосомных частиц является принципом организации хроматина (см.) как в интерфазной, так и в метафазной хромосоме.
В геноме эукариот (см. Геном) выделяют несколько классов ДНК по числу повторяющихся последовательностей нуклеотидов, составу последовательностей, их размерам. У человека ДНК может быть подразделена на ДНК с многократно повторяющимися последовательностями нуклеотидов, включая сателлитную ДНК (ок. 10,3%), ДНК с умеренно повторяющимися последовательностями (ок. 12,3%), ДНК с низкой их повторяемостью (13,4%), а также ДНК, состоящую из уникальных последовательностей (около 64%). У человека четыре основных типа сателлитных ДНК локализуются в большинстве хромосом, но неодинаково распределяются по типам и количеству. ДНК с многократно повторяющимися последовательностями содержится преимущественно в гетерохроматине (сильно спирализованных и интенсивно окрашенных районах хромосомы). На поперечник хромосомы при ее максимальной деконденсации приходится одна молекула ДНК. В метафазной хромосоме составляющая ее молекула ДНК должна укоротиться в 104 раз по сравнению с ее длиной в свободном от белков состоянии. Взаимодействие ДНК с гистонами при формировании нуклеосом и нити диаметром 10 нм обеспечивает укорочение исходной нити ДНК примерно в 6,5—7 раз и увеличение диаметра с 3 нм до 10 нм. В нативном хроматине преобладают нити второго порядка диаметром 20—30 нм, в фибриллах этого уровня общее укорочение ДНК оказывается примерно 40-кратным.
ДНК с умеренным числом повторов обнаруживается главным образом в G-окрашивающихся сегментах. С помощью флюорохромов (см.), по-разному связывающихся с аденинтимин и гуанинцитозин парами оснований ДНК, показано различие участков метафазной хромосомы по составу оснований. Специфичность ДНК в разных участках хромосом, вероятно, определяет их различие по генетической активности.
Классификация
Числовой CIN — это высокая скорость увеличения или потери целых хромосом; вызывая анеуплоидию . Нормальные клетки допускают ошибки в сегрегации хромосом в 1% клеточных делений, тогда как клетки с CIN делают эти ошибки приблизительно в 20% клеточных делений. Поскольку анеуплоидия является общим признаком опухолевых клеток, наличие анеуплоидии в клетках не обязательно означает наличие CIN; высокий уровень ошибок является определяющим для CIN. Один из способов дифференциации анеуплоидии без CIN и анеуплоидии, вызванной CIN, заключается в том, что CIN вызывает широко вариабельные (гетерогенные) хромосомные аберрации; тогда как, когда CIN не является причинным фактором, хромосомные изменения часто более клональны.
Структурная CIN отличается тем, что фрагменты хромосом могут быть дублированы или удалены, а не целые хромосомы. Перестройка частей хромосом ( транслокации ) и амплификации или делеции в хромосоме также могут происходить в структурной CIN.
Симптомы, возникающие при синдроме ломкой Х-хромосомы
Отсутствие или снижение уровня функционального белка FMRP, вызванное мутацией гена FMR1, приводит к симптомам заболевания, которые постепенно развиваются от рождения до полового созревания.
У новорожденных и младенцев мужского пола, страдающих синдромом FraX:
- низкий вес при рождении;
- небольшая окружность головы;
- увеличенный объем яичка;
- большие ушные раковины;
- мышечная гипотензия (снижение мышечного тонуса).
У детей наблюдается следующее:
- нарушения речи;
- задержка психомоторного развития;
- симптомы аутизма (например, боязнь общения, кусание рук, нарушение осязания).
У взрослых мужчин бывают:
- черепно-лицевые деформации (большие ушные раковины, большая нижняя челюсть, высокое небо);
- бледно-голубые радужные оболочки также характерны для синдрома ломкой Х-хромосомы;
- увеличение яичек;
- деформация позвоночника;
- широкие руки;
- короткие пальцы;
- эпилептические припадки.
Среднее значение IQ у мужчин с полной мутацией составляет около 40 – они демонстрируют нарушение координации глаз и рук, нарушение памяти или трудности с решением проблем.
У женщин с полной мутацией симптомы намного слабее, чем у мужчин, и связаны в первую очередь с повышенным риском эмоциональных расстройств.
Больные женщины:
- имеют IQ в пределах нормы или проявляют признаки умеренной умственной отсталости (IQ около 50-69);
- в среднем у 35% из них наблюдаются такие симптомы, как черепно-лицевые изменения, замедленность движений, проблемы с произношением определенных слов или нарушения концентрации внимания.
Нарушение концентрации внимания
Однако у некоторых женщин с полной мутацией симптомы могут вообще не проявляться из-за избирательной инактивации аномальной Х-хромосомы.
У носителей болезни обычно нет симптомов, подтверждающих их носительство. Некоторые женщины (около 20% носителей) испытывают преждевременное снижение функции яичников, что вызывает бесплодие у женщин, так как оно связано с более ранней менопаузой (до 40 лет). У некоторых мужчин с перестановкой могут развиться неврологические проблемы (нарушение памяти, судороги).
Как это касается других членов семьи
Если у одного из членов семьи обнаружена хромосомная перестройка, возможно, Вы захотите обсудить этот вопрос с
другими членами семьи. Это даст возможность другим родственникам, при желании, пройти обследование (анализ
хромосом в клетках крови) для определения носительства хромосомной перестройки
Это может быть особенно важно для
родственников, уже имеющих детей или планирующих беременность. Если они не являются носителями хромосомной
перестройки, они не могут передать ее своим детям
Если же они являются носителями, то им могут предложить пройти
обследование во время беременности для анализа хромосом плода.
Некоторым людям сложно обсуждать проблемы, связанные с хромосомной перестройкой, с членами семьи. Они могут
бояться причинить беспокойство членам семьи. В некоторых семьях люди из-за этого испытывают сложности в общении и
теряют взаимопонимание с родственниками. Врачи-генетики, как правило, имеют большой опыт в решении подобных
семейных ситуаций и могут помочь Вам в обсуждении проблемы с другими членами семьи.
Флуоресцентная гибридизация in situ (FISH)
Аббревиатура FISH расшифровывается как fluorescent in situ hybridization – флуоресцентная гибридизация на месте. Это цитогенетический метод, который применяют для выявления и определения положения специфической последовательности ДНК на хромосомах. Для этого используют специальные зонды — нуклеозиды, соединенные с флуорофорами или некоторыми другими метками. Визуализацию связавшихся ДНК-зондов проводят при помощи флуоресцентного микроскопа.
Метод FISH позволяет изучать небольшие хромосомные перестройки, которые не идентифицируются при стандартном исследовании кариотипа. Однако, имеет один существенный недостаток. Зонды являются специфичными только к одному участку генома и, как следствие, при одном исследовании можно определить наличие или число копий только этого участка (или нескольких при использовании многоцветных зондов). Поэтому важным является правильная клиническая предпосылка, а FISH анализ может только подтвердить иди не подтвердить диагноз.
Альтернативой этому методу является хромосомный микроматричный анализ, который при такой же точности, чувствительности и специфичности определяет количество генетического материала в сотнях тысяч (и даже миллионах) точек генома, что дает возможность диагностики практически всех известных микроделеционных и микродупликационных сииндромов.
Что такое изменчивость?
Изменчивость — свойство живых организмов: потомки приобретают признаки, отличающие их от предков. Этот термин достаточно общий, поэтому поделим его на типы и охарактеризуем каждый из них. Это позволит лучше разобраться, какой может быть изменчивость в ЕГЭ по биологии
Обратите на эту тему внимание: профессии, связанные с генетикой, явно будут востребованы в ближайшие годы!
Не знаете, какой вуз выбрать? Что это такое? Все просто: вы расскажете о себе и о своих интересах
А специалист посоветует, на какие специальности обратить внимание, в какой вуз поступать, какие ЕГЭ сдавать. Так вы сэкономите время на подготовку и сможете выбрать образование, которое точно окажется для вас интересным и полезным!
Ненаследственная изменчивость
Признаки не передаются потомкам по наследству. Подумайте: если хорошо кормить домашнюю кошку, родятся ли ее котята самыми упитанными? Конечно, нет.
У этой разновидности изменчивости есть еще несколько синонимичных названий. Например, фенотипическая, так как изменения затрагивают только фенотип (внешнее проявление признака). Еще одно название — групповая, она проявляется сходно у всех особей группы, допустим, целая группа людей поехала в отпуск к морю, и все члены этой группы долгое время провели под солнечными лучами. У каждого из них кожа изменит цвет: кто-то обгорит, кто-то сразу загорит, но изменит у всех. Так же эту изменчивость называют модификационной, а все изменения, не затрагивающие генотип — модификациями.
Еще одно название предложил Чарльз Дарвин, который не знал почти ничего о наследовании генов. Он ввел термин «определенная изменчивость». Такие изменения можно предугадать. Безусловно, если мы будем лежать на диване дни напролет, то процент жировой ткани в организме увеличится, а если каждый день будем выходить на пробежку, увеличится процент мышечной ткани.
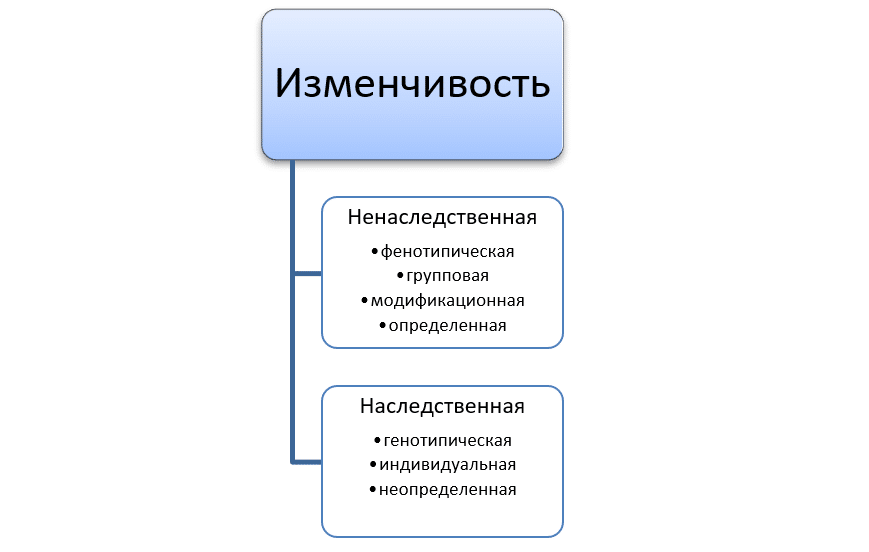
Наследственная изменчивость
Второй тип изменчивости является абсолютной противоположностью модификационной. Она называется наследственной, так как передается от предков потомкам. По аналогии с первым типом, ее еще называют генотипической: она затрагивает генотип. Такая изменчивость проявляется у каждого организма по-своему, индивидуально, поэтому есть термин «индивидуальная изменчивость». Например, в одной семье, у одних родителей могут родиться два сына: один дальтоник, а второй с нормальным цветовым зрением. Ну и разве мог Дарвин остаться в стороне? Для этой изменчивости он предложил название — неопределенная, ведь нельзя однозначно предсказать у какого организма какие изменения проявятся.
Но на этом разновидности изменчивости не заканчиваются. Наследственную изменчивость можно разделить еще на два типа.
1. Комбинативная изменчивость
Представьте себе калейдоскоп, внутри которого несколько цветных стеклышек. Когда вы смотрите в него, то каждый раз видите разные узоры, но новые стеклышки внутрь не досыпаются. Вот и такая изменчивость возникает при сочетании уже имеющихся генов. В случае, если у темноволосых родителей рождается светловолосый ребенок, перед нами пример комбинативной изменчивости.
Перечислим основные причины, в результате которых происходят комбинации. Первая причина — это кроссинговер (обмен участками гомологичных хромосом), происходящий в профазе первого деления мейоза. А вторая — это случайный подбор родительских пар. Нельзя точно предсказать какой из самцов павлина победит в половом отборе, чей хвост в этом году будет самым красивым. Третья причина — это случайная встреча гамет, никто не знает, какой именно сперматозоид оплодотворит каждую из яйцеклеток и оплодотворит ли вообще. Четвертая причина – это расхождение хромосом в мейозе.

Мутационная изменчивость
Второй тип наследственной изменчивость – это мутационная изменчивость. Она бывает вызвана воздействием на организм мутагенов, а в основе ее лежит изменение структуры ДНК или хромосом.
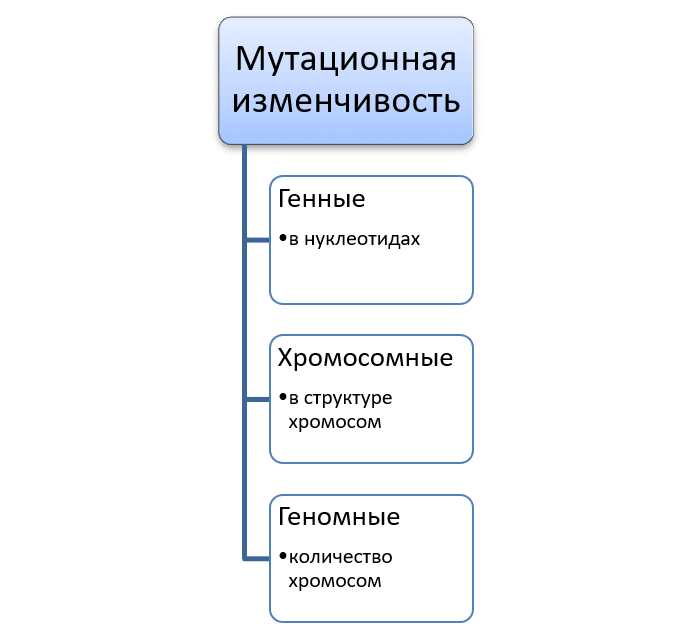
Мутационная изменчивость тоже делится на
несколько типов. Она бывает генной, хромосомной и геномной. Генные мутации связаны с изменением
нуклеотидов в гене (выпадение, удвоение, замена и т.д.). Хромосомные мутации связаны с изменением в структуре в хромосом
(утрата плеча, выпадение участка, поворот участка на 180 градусов, удвоение
участков и т.д. ). Геномные мутации
связаны с изменением числа хромосом.
Только что мы повторили всю теорию, затрагивающую изменчивость в ЕГЭ по обществознанию! Теперь я предлагаю перейти к практике и разобрать задания, аналогичные тем, которые могут встретиться на ЕГЭ.
Скрининг на генетические заболевания
Сегодня известно более 11 000 моногенных заболеваний, которые кодируются одним геном (генетически обусловленные) и передаются от родителей их потомкам. Механизм передачи многих генетических болезней объясняется принципами Менделя.
Аутосомно-доминантные моногенные синдромы встречаются с частотой 1: 200 индивидов; заболевание наблюдается у многих поколений, передается потомкам и рецидивирует с частотой 50%. Примерами аутосомно-доминантных моногенных расстройств могут быть:
- ахондроплазия,
- нейрофиброматоз,
- синдром Марфана,
- болезнь Хантингтона,
- семейный полипоз.
Появление аутосомно-доминантных заболеваний у новорожденных от «здоровых» родителей может быть обусловлено следующими причинами:
1. Мозаицизм зародышевых клеток. Мутация может иметь место лишь в популяции зародышевых клеток. Итак, родители являются непораженными, но могут передавать мутацию потомкам.
2. Новые мутации. Рост возраста родителей ассоциируется с увеличением риска аутосомно-доминантных расстройств (ахондроплазии, танатофорной дисплазии, нейрофиброматоза, синдрома Аперта — краниосиностоз). Риск рецидивов у других детей не увеличивается.
3. Вариабельна экспрессия. Тяжесть заболевания может варьировать, и родители могут не распознать мягкие и субклинические мутации.
4. Уменьшенная пенетрантность. Родители могут иметь аномальный ген без клинических проявлений заболевания.
5. Неверное отцовство. Частота неверного отцовства достигает 15%.
Аутосомно-рецессивные моногенные заболевания проявляются в многочисленных родственников при наличии двух пораженных аллелей. Если оба родителя являются носителями пораженного гена, риск заболевания у потомства равен 25% при каждой беременности. Аутосомно-рецессивные заболевания включают кистозный фиброз, серповидно-клеточную анемию, фенилкетонурию, болезнь Тея-Сакса, Канавана и др.
При Х-сцепленных рецессивных синдромах (гемофилия и др.) мать-носитель пораженного гена передает его своим сыновьям. Итак, 50% сыновей могут быть больными и 50% дочерей будут носителями этого гена. Редкие Х-доминантные синдромы могут передаваться от каждого родителя каждому ребенку подобно аутосомно-доминантных синдромов. Фенотип может сильно варьировать, что связано со смешанной пенетрантностью, лионизацией (гетерохроматизацией) Х-хромосомы (синдром ломкой Х-хромосомы) и геномным импринтингом.
Экспансия тринуклеотидных повторов. Некоторые гены содержат участки тройных повторов (например, ССС). Такие участки являются нестабильными и могут увеличиваться в следующих генерациях, этот феномен получил название антиципации. Количество повторений определяет степень поражения индивида. Экспансия тринуклеотидных повторов составляет основу многочисленных генетических расстройств, таких как синдром ломкой (фрагильной) Х-хромосомы, миотоническая дистрофия и болезнь Хантингтона.
Синдром ломкой (фрагильной) Х-хромосомы является наиболее частой причиной семейной задержки умственного развития. Пораженные мужчины имеют типичные черты: большие уши, выступающая челюсть, большие яички, аутичное поведение, легкая или умеренная умственная отсталость. Женщины обычно менее поражены в связи с инактивацией Х-хромосомы.
Ген ломкой Х-хромосомы локализуется в Х-хромосоме и имеет три нуклеотидные повтора (ССС). Нормальные индивиды имеют 6-50 повторов, непораженные носители женского пола могут иметь 50-200 повторов, которые могут распространяться на мейоза до полной мутации при наличии более 200 повторов. Если имеет место полная мутация, ген инактивируется путем метилирования; плод будет пораженным. Тяжесть заболевания зависит от степени Х-инактивации у женщин, степени метилирования и мозаицизма размера повторов.
Женщины-носители премутации имеют 50%-й риск передачи гена с экспансией. Мужчины с премутациею фенотипически являются нормальными, но все их дочери будут носителями премутации. В случае трансмиссии мужчинам количество повторов остается стабильным. Тест на ломку Х-хромосому выполняется с целью выявления количества повторов и степени метилирования.
Хромосомные аберрации в опухолях солидного типа
Солидные опухоли состоят из большого числа недифференцированных клеток, которые склонны к активному делению. Данный тип рака развивается из эпителиальной ткани и характеризуется высокой агрессивностью. Среди примеров вариаций числа копий генов в опухоли солидного строения можно отметить:
- амплификацию гена ERBB2 (он же Her-2/neu). Данный вид мутации имеет большое значение в развитии рака молочной железы и влияет на тактику лечения данного заболевания. Амплификация ERBB2 выявляется примерно у каждой третьей пациентки;
- транслокацию ROS1 и EML4-ALK. В большинстве случаев возникает при немелкоклеточном раке легкого. Выявление данного вида хромосомной аберрации в опухоли оказывает влияние на назначение таргетной терапии, в частности, препарата «Кризотиниб»;
- транслокацию гена RET. Этот ген отвечает за кодирование белка, относящегося к классу рецепторных тирозинкиназ. Транслокации в нем выявляются при эндокринных неоплазиях, раке щитовидной железы, феохромоцитоме, немелкоклеточном раке легкого и других опухолях. Как и в предыдущем случае, диагностика транслокации гена RET позволяет определиться с выбором препарата для таргетной терапии;
- хромосомные аберрации при опухолях головного мозга. Могут выявляться в генах семейства EGFR, VEGFR, PDGFR, C-KIT, BRAF и т.д. Выявление подобных изменений позволяет определить генетический подтип опухоли головного мозга, спрогнозировать клиническое течение, ответ на химиолучевую терапию и определить чувствительность к специфичным лекарственным препаратам.
Выявление описанных выше вариаций числа копий в опухоли солидного типа имеет важное диагностическое значение, поскольку позволяет определиться с тактикой лечения. По этой причине подобные исследования все чаще входят в программу обследования онкологических пациентов
Известные заболевания хромосомной природы
Одним из самых известных заболеваний, происходящих по причине наличия аномалий в генетическом материале, является синдром Дауна. Он обуславливается трисомией по 21 хромосоме. Характерным признаком этой болезни является отставание в развитии. Дети испытывают серьезные проблемы во время обучения в школе, часто им требуется альтернативная методика преподавания материала. Вместе с тем отмечаются нарушения физического развития – плоское лицо, увеличенные глаза, клинодактилия и другие. Если такие люди прикладывают значительные усилия, они могут достаточно хорошо социализироваться, известен даже случай успешного получения высшего образования мужчиной с синдромом Дауна. У больных повышен риск заболеть деменцией. Это и ряд других причин приводит к небольшой продолжительности жизни.
К трисомии относится и синдром Патау, только в этом случае имеется три копии 13 хромосомы. Для заболевания характерны множественные пороки развития, часто с полидактилией. В большинстве случаев отмечается нарушение деятельности центральной нервной системы либо ее неразвитость. Часто (примерно в 80 процентах) больные имеют пороки развития сердца. Тяжелые нарушения приводят к высокой смертности – в первый год жизни умирает до 95% детей с этим диагнозом. Заболевание не поддается лечению или коррекции, как правило, можно лишь обеспечить достаточно постоянный контроль состояния человека.
Еще одна форма трисомии, с которой рождаются дети, относится к 18 хромосоме. Заболевание в этом случае носит название синдрома Эдвардса и характеризуется множественными нарушениями. Деформируются кости, часто наблюдается измененная форма черепа. Сердечно-сосудистая система обычно с пороками развития, также проблемы отмечаются с органами дыхания. В результате около 60% детей не доживают до 3 месяцев, к 1 году умирает до 95% детей с этим диагнозом.
Трисомия по другим хромосомам у новорожденных практически не встречается, поскольку почти всегда приводит к преждевременному прерыванию беременности. В части случаев рождается мертвый ребенок.
С нарушениями числа половых хромосом связан синдром Шерешевского-Тернера. Из-за нарушений в процессе расхождения хромосом теряется X-хромосома в женском организме. В результате организм не получает должного количества гормонов, поэтому нарушается его развитие. В первую очередь это относится к половым органам, которые развиваются лишь отчасти. Практически всегда для женщины это обозначает невозможность иметь детей.
У мужчин полисомия по Y или X хромосоме приводит к развитию синдрома Клайнфельтера. Для этого заболевания характерна слабая выраженность мужских признаков. Зачастую сопровождается гинекомастией, возможно отставание в развитии. В большинстве случаев наблюдаются ранние проблемы с потенцией и бесплодие. В этом случае, как и для синдрома Шерешевского-Тернера, выходом может стать экстракорпоральное оплодотворение.
Виды хромосомных мутаций
- Делеция — утрата части хромосомы.
- Дефишенси — утрата концевого участка.
- Дупликация — удвоение части хромосомы.
- Амплификация — многократное повторение.
- Инсерция — вставка хромосомного участка.
- Инверсия — поворот участка хромосомы на 180°. Перицентрическая инверсия — поворот участка, содержащего центромеру; парацентрическая — не содержащего центромеру.
- Транслокация — перенос участка с одной хромосомы на другую.В частности реципрокная транслокация — обмен участками между негомологичными хромосомами; робертсоновская транслокация — соединение двух акроцентрических хромосом, в результате чего образуется одна метацентрическая (равноплечая) или субметацентрическая.
Если дефишенси происходит на обоих концах хромосомы, то это может привести к образованию кольцевой хромосомы.
В результате хромосомных мутаций могут возникать хромосомы с двумя центромера или не содержащие ни одной.
Хромосомы без ценромер называются ацентрическими фрагментами и обычно теряются при делении клетки. Хромосомы с двумя центромерами называются дицентрическими (дицентриками). В анафазе они формируют так называемые мосты и разрываются. В последствии в клетке они образуют хроматиновые тельца (микроядра).
Если в результате хромосомной мутации не произошло добавления или потери генетического материала, то такие перестройки называются сбалансированными и обычно не приводят к каким-либо последствиям.
В результате несбалансированной перестройки происходит добавление или потеря генетического материала, и организмы могут иметь выраженные отклонения.
При инверсиях порядок генов в участке хромосомы меняется на обратный. Фенотипически подобная мутация обычно не проявляется.
Однако при мейозе в результате кроссинговера могут образовываться гаметы с несбалансированным генетическим материалом.
Хромосомные мутации возникают как в половых, так и соматических клетках. В первом случае чаще всего приводят к врожденным заболеваниям, потере фертильности.
Хромосомные перестройки в соматических клетках могут привести к онкологическим заболеваниям. Удачные для организма хромосомные мутации редки, но играют важную роль в эволюционном процессе, приводят к образованию новых видов.
Хромосомные мутации возникают из-за возникновения в клетках двунитевых разрывов ДНК, которые не были нормально восстановлены.
Такие разрывы происходят как спонтанно, так и под действием мутагенов (например, ионизирующего излучения).
Мутационная изменчивость. Классификация мутиций
В этом случае наблюдаются потеря (делеция) или удвоение части (дупликация) генетического материала одной или нескольких хромосом, изменение ориентации сегментов хромосом в отдельных хромосомах (инверсия), а также перенос части генетического материала с одной хромосомы на другую (транслокация) (крайний случай — объединение целых хромосом.
На генном уровне изменения первичной структуры ДНК генов под действием мутаций менее значительны, чем при хромосомных мутациях, однако генные мутации встречаются более часто.
В результате генных мутаций происходят замены, делеции и вставки одного или нескольких нуклеотидов, транслокации, дупликации и инверсии различных частей гена. В том случае, когда под действием мутации изменяется лишь один нуклеотид, говорят о точечных мутациях
Антимутационные механизмы обеспечивают обнаружение, устранение или подавление активности онкогенов. Реализуются антимутационные механизмы при участии онкосупрессоров и систем репарации ДНК.
Человек как объект генетических исследований.
Цитогенетический метод; его значение для диагностики хромосомных синдромов. Правила составления идиограмм здоровых людей. Идиограммы при хромосомных синдромах(аутосомные и гоносомных).
Примеры.
Человек, как объект генетических исследований представляет сложность:
- Нельзя принимать гибридологический метод.
- Медленная смена поколения.
- Малое кол-во детей.
- Большое число хромосомю
Цитигенетический метод (основан на изучеии кариотипа).
Кариотип изучают на метофазных пластинках в культуре лимфаитов крови. Метод позволяет диагностировать хромосомные болезни, появляющиеся в результате геномных и хромосомных мутаций.
Цитологический контроль необходим для диагностики хромо-сомных болезней, связанных с ансуплоидией и хромосомными мутациями. Наиболее часто встречаются болезнь Дауна(трисомия по 21-й хромосоме), синдром Клайнфелтера (47 XXY), синдром Шершевского — Тернера (45 ХО) и др.
Потеря участка одной из гомологичных хромосом 21-й пары приводит к заболеванию крови — хроническому миелолейкозу.
При цитологических исследованиях интерфазных ядер со-матических клеток можно обнаружить так называемое тельце Барри, или половой хроматин.
Оказалось, что половой хроматин в норме есть у женщин и отсутствует у мужчин. Он представляет собой результат гетерохроматизации одной из двух Х-хромосом у женщин. Зная эту особенность, можно идентифицировать половую принадлежность и выявлять аномальное количество Х-хромосом.
Выявление многих наследствен-ных заболеваний возможно еще до рождения ребенка.
Метод пренатальной диагностики заключается в получении околоплодной жидкости, где находятся клетки плода, и в последующем биохимическом и цитологическом определении возможных наследственных аномалий. Это позволяет поставить диагноз на ранних сроках беременности и принять решение о се продолжении или прерывании
Биохимический метод изучения генетики человека; его значение для диагностики наследственных болезней обмена веществ. Роль транскрипционных, посттранскрипционных и посттрансляционных модификаций в регуляции клеточного обмена.
Проблемы методики
Опухоли неоднородны. Они состоят из разных клеток, которые могут отличаться весьма значительно. И, например, в 80% клеток опухоли мутация определенного гена присутствует, а 20% клеток поделились с другим распределением хромосом — и остались немутировавшими. Да, мы назначаем препарат по результатам молекулярно-генетического теста, и против 80% опухолевых клеток он сработает эффективно, но для оставшихся 20% нужно будет придумывать другое лечение.
Некоторые виды рака более-менее гетерогенны, например, РМЖ. А некоторые опухоли, такие как саркомы, напоминают по структуре винегрет. Это затрудняет и диагностику, и лечение: нельзя заранее узнать, в какой части опухоли какие клетки, сколько их видов, как сильно они отличаются. И нельзя, грубо говоря, взять 10 образцов из разных мест опухоли — по ним придется сделать 10 отдельных генетических исследований.
До 30% таргетных и иммунопрепаратов в России назначается без соответствующего обоснования — без исследований генетики опухоли. И часть этих лекарств оказывается пустой тратой средств бюджета и денег пациента, потому что назначать таргетное лечение без понимания генетики опухоли — это рулетка: зарегистрировано более 600 препаратов. Например, для рака молочной железы есть пять протоколов лечения, в зависимости от мутации гена HER2/Neu.
В западной медицине определение генетического профиля опухоли уже становится стандартом лечения. Для российских онкопациентов молекулярно-генетические тестирования — все еще редкий случай, к сожалению — для бюджетной медицины это пока дорого. Но есть надежда, что все изменится к лучшему. Если сейчас оно стоит 600 тыс. руб., то 5 лет назад стоило больше миллиона — технология становится все проще и совершеннее, а, значит, популярнее и доступнее. Здесь время работает на нас.
Большинство онкологов в России НЕ используют молекулярно-генетические тесты. Потому что не имеют достаточного опыта работы с ними и специфических знаний. Не получится просто открыть отчет и «списать» оттуда лечение
Нужно принимать во внимание множество факторов, понимать, как все эти многочисленные мутации влияют друг на друга, на рост опухоли, на потенциальную индивидуальную переносимость пациентом препарата и т. п
Поэтому мало просо сделать генетический тест, нужно уметь понять результаты и сделать верные выводы. Мы с коллегами чаще всего сначала изучаем отчет сами (бывает, приходится посидеть над ним дома, в тишине после работы) — а потом еще и собираем консилиум, принимаем коллегиальное решение.
Необходимо продумывать комбинации из таргетных препаратов, уметь сочетать их химиотерапевтическими лекарствами, предусматривать возможные побочные эффекты таких «коктейлей». Это довольно сложная задача — и врач должен быть очень мотивирован постоянно учиться.
Но хорошие истории пациентов, честно говоря, всегда мотивируют лучше всего.
Сейчас у нас есть пациентка, 48 лет, с рецидивирующей глиобластомой (агрессивная опухоль мозга). К нам она попала после того, как прошла две линии терапии в государственном онкоцентре. Там все делали правильно, проводили лучевую терапию и назначали таргетный препарат, но опухоль все равно вернулась. Женщине отвели полгода жизни.
Мы предложили ей полное молекулярно-генетическое тестирование. Да, оно стоит 600 тыс. рублей, сокращенный вариант, за 250, в ее случае не подошел — нужно было расширенное тестирование, с максимально полным набором мутаций.
Но по результатам обследования назначили ей препарат, который предназначен обычно для лечения немелкоклеточного рака легкого. Он эффективен против опухолей с мутацией EGRF — у нашей пациентки глиобластома была именно с этой мутацией.
Женщина ходит к нам лечиться и наблюдаться уже 4 года. Это в 5 раз дольше, чем при стандартной терапии. Причем, она самостоятельна, живет эти 4 года обычной жизнью, ходит на работу и собирается дождаться внуков.
Так что, хоть нам в «Медицине 24/7» и приходится все время держать мозги в тонусе, разбираться в новых и новых исследованиях генетических мутаций — результаты определенно того стоят.
Будьте здоровы.
Материал подготовлен заместителем главного врача по лечебной работе клиники «Медицина 24/7», кандидатом медицинских наук Сергеевым Петром Сергеевичем.